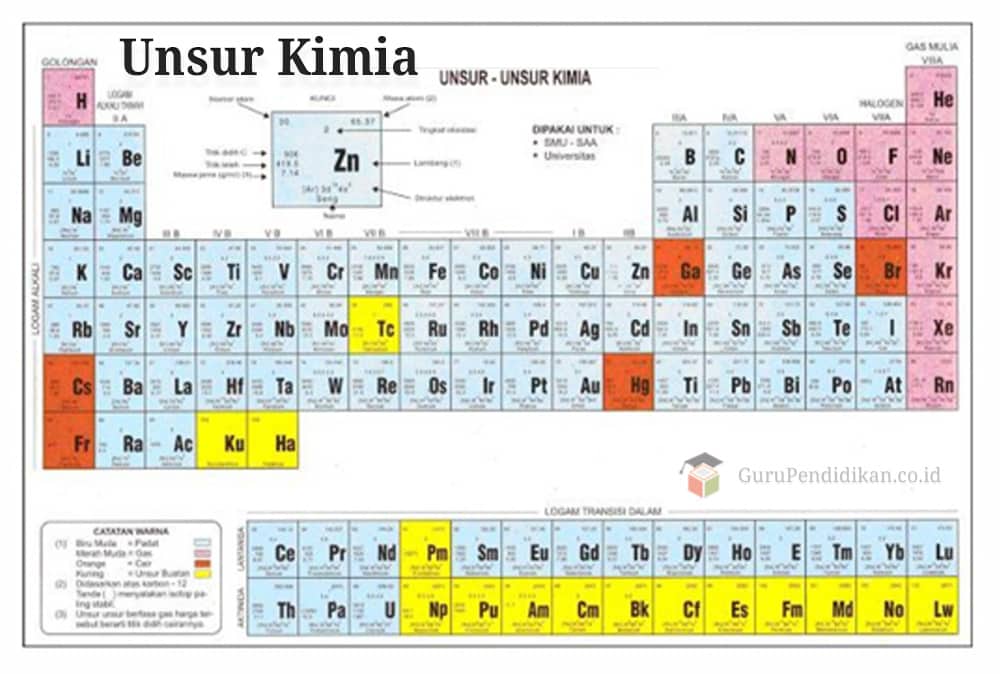
Pengertian Unsur Kimia
Unsur merupakan suatu zat yang hanya mengandung satu jenis atom. Variasi yang luar biasa disekeliling kita tersusun dari substansi-substansi yang juga bisa disebut dengan unsur. Singkatnya Unsur merupakan bahan murni yang tidak dapat dipecah menjadi lebih sederhana lagi.
Unsur harus berkombinasi dahulu baru bisa membentuk senyawa, Kebanyakan unsur membentuk kombinasi dua, tiga, atau lebih, untuk membentuk senyawa. Karena pengetahuan tentang unsur ini menarik perhatian saya, saya mencoba untuk membaginya dengan sobat semua dalam postingan ini. Dua hal utama yang akan saya bahas adalah tentang Asal mula unsur dan Pengelompokkannya. Jika ingin terlibat lebih dalam mari dibaca dengan seksama.
Unsur adalah zat murni yang dapat diuraikan lagi menjadi zat lain yang lebih sederhana dengan reaksi kimia biasa, Senyawa adalah zat yang terbentuk dari penggabungan unsur-unsur dengan pembagian tertentu. Senyawa dihasilkan dari reaksi kimia antara dua unsur atau lebih melalui reaksi pembentukan. Misalnya, karat besi (hematit) berupa Fe2O3 dihasilkan oleh reaksi besi (Fe) dengan oksigen (O).
Senyawa dapat diuraikan menjadi unsur-unsur pembentuknya melalui reaksi penguraian. Senyawa mempunyai sifat yang berbeda dengan unsur-unsur pembentuknya. Senyawa hanya dapt diuraikan menjadi unsur-unsur pembentuknya melalui reaksi kimia. Pada kondisi yang sama, senyawa dapat memiliki wujud berbeda dengan unsur-unsur pembentuknya. Sifat fisika dan kimia senyawa berbeda dengan unsur-unsur pembentuknya. Misalnya reaksi antara gas hidrogen dan gas oksigen membentuk senyawa air yang berwujud cair.
Baca Juga Artikel Yang Mungkin Berhubungan : Pengertian Reaksi Kimia
Asal Mula Unsur
Sampai saat ini, sudah ditemukan sekitar 115 unsur di bumi ini. Nah kira-kira darimana ya unsur-unsur itu berasal? Menurut sumber yang saya baca sih dikatakan Seluruh unsur di Bumi terbentuk dari jantung bintang yang meledak.
Jagat raya yang pertama pertama terbentuk hanya terdiri dari dua unsur, yaitu helium dan hidrogen yang membentuk bintang, pada inti bintang-bintang ini, hidrogen dan helium bersama-sama membentuk unsur baru yang lebih berat, bahkan unsur yang lebih berat dihasilkan dalam ledakan bintang besar yang disebut supernova.
Baca Juga Artikel Yang Mungkin Berhubungan : √ Makalah Ikatan Kimia : Pengertian, Jenis Beserta Gambarnya Lengkap
Jenis Pengelompokkan Unsur
Dengan berdasarkan penemuannya, unsur tersebut dikelompokkan kedalam 2 kelompok, yakni
- Unsur Alami merupakan unsur yang murni,
- Unsur Buatan yang dibuat didalam suatu laboratorium dan juga biasanya berusia pendek
Unsur Alami
Seperti dipenjelasan diatas , sampai sekarang ini sudah ditemukan 115 unsur, 90 dari itu adalah unsur yang alami. Pada tiap-tiap substansi di bumi tersebut tersusun atas satu atau juga lebih dari 90 unsur ini. Oksigen adalah salah satu unsur yang paling umum di bumi, serta juga juga manfaatnya yang paling kita ketahui adalah unsur pernapasan bagi kehidupan manusia (bernafas), Sedangkan Hidrogen adalah suatu unsur yang paling banyak di jagat raya.
Unsur Buatan
Secara alami, tidak terdapat unsur yang lebih berat selain uranium, tetapi para peneliti mampu untuk dapat menciptakan unsur baru yang lebih berat,caranya ialah dengan menggabungkan dua unsur yang lebih kecil bersama-sama didalam kecepatan yang tinggi, Namun kebanyakan dari unsur baru tersebut tidak bertahan lama serta juga cepat pecah.
Baca Juga Artikel Yang Mungkin Berhubungan : Tabel Periodik Unsur Kimia
Sifat-sifat Unsur
Selain dari Pengelompokkan di atas, Unsur Tersebut juga dikelompokkan dengan berdasarkan sistem periodik unsur oleh para ilmuan, untuk lebih mudah dibedakan menurut sifatnya.Berikut ini merupakan pengelompokkannya yang terbagi menjadi ialah sebagai berikut
- unsur logam,
- nonlogam,
- semi logam.
Unsur-unsur Logam
Sebagian besar atas unsur yang sudah ditemukan itu merupakan unsur logam, kira-kira sekitar 3/4 dari keseluruhan unsur. Kebanyakan unsur logam tersebut mempunyai kerapatan yang tinggi, serta juga mengkilap. Unsur-unsur tersebut memiliki banyak kegunaan, dikarenakan unsur tersebut kuat, meskipun kuat unsur tersebut tetap mudah untuk dibentuk. Selain itu juga, logam juga adalah suatu penghantar panas serta juga listrik yang baik.
Unsur-unsur Nonlogam
Terdapat kurang lebih 16 unsur nonlogam yang terbentuk engan secara alami. Semuanya (kecuali grafit) adalah suatu penghantar panas serta juga listrik yang buruk, sifat yang dipunyainya ini bertolak belakang dengan unsur-unsur logam. Pada suhu kamar, 4(empat) unsurnya (fosfor, karbon, sulfur, serta iodin) berupa padatan, 11(sebelas) lainnya berupa gas.
Unsur-unsur Semilogam
Unsur-unsur semilogam tersebut disebut juga dengan metaloid, dapat untuk bertindak sebagai penghantar yang buruk (seperti nonlogam), tetapi juga bisa dibuat supaya menjadi penghantar yang baik (seperti layaknya logam). dikarenakan sifatnya tersebut, unsur-unsur semilogam disebut juga dengan semikonduktor. Terdapat 9(sembilan) unsur semilogam, serta semuanya berupa padatan disuhu kamar.
Baca Juga Artikel Yang Mungkin Berhubungan : Pengertian Ilmu Kimia
Fungsi dan manfaat Unsur dan Senyawa
Unsur-unsur utama dalam bentuk unsur atau senyawa memiliki banyak kegunaan dalam kehidupan kita sehari-hari. Mari kita pelajari kegunaan beberapa unsur dan senyawa dari unsur golongan utama.
Golongan Alkali
- Unsur Natrium
Natrium memiliki kemampuan daya gabung terhadap oksigen besar, sehingga sangat mudah terbakar di udara. Oleh karena itu, Na disimpan dalam minyak tanah atau dalam parafin cair. Natrium terbakar dengan nyala kuning. Natrium banyak digunakan untuk pembuatan lampu-lampu natrium dan pembuatan senyawa-senyawa organik. -
Senyawa Natrium Hidroksida
Natrium hidroksida (NaOH), disebut juga soda api atau soda kaustik. NaOH adalah suatu basa yang sangat kuat; larut dengan baik dalam air dengan menimbulkan kalor (larutannya dinamakan lindi natron); mengikat CO2 dari udara dan berubah menjadi Na2CO3. Soda api digunakan dalam membuat “sabun keras”, membersihkan minyak tanah, dan dalam industri. -
Senyawa Natrium Klorida
Natrium klorida (NaCl) penting sebagai bahan makanan, dan pengawet sayur, daging, telur, dan ikan. Penambahan NaCl dalam air es digunakan sebagai pendingin dalam pembuatan bermacam-macam es, misal es puter, es lilin, dan es krim. Dalam industri, NaCl digunakan sebagai sumber unsur Na dan Cl, dan sebagai bahan pembuatan senyawan-senyawa lain yang mengandung Na atau Cl, seperti asam klorida, dan soda. NaCl dalam industri keramik dipakai sebagai campuran bahan glasir. -
Senyawa Natrium Karbonat
Natrium karbonat (soda) mudah larut dalam air, dan larutannya bersifat basa. Berdasarkan sifat inilah maka soda digunakan sebagai zat pencuci. Soda digunakan dalam perusahaan pencucian untuk menghilangkan noda minyak. Soda juga dipakai dalam industri kaca, dan untuk melunakkan air sadah. -
Senyawa Natrium Hidrogen Karbonat
Natrium hidrogen karbonat dipakai dalam alat pemadam api. Alat ini diisi dengan larutan NaHCO3 dicampur dengan saponin, suatu zat dapat berbuih. Fungsi lain NaHCO3 adalah untuk menghilangkan bau tengik dari mentega; mengembangkan kue; menghilangkan lemak dan lilin dalam pencucian bulu domba; serta menghilangkan gom dari sutra. -
Senyawa Natrium Nitrat atau Sendawa Chili
Natrium nitrat dipakai sebagai pupuk buatan dan pembuatan asam sendawa. -
Senyawa Kalium Nitrat
Kalium nitrat berupa hablur-hablur putih, tidak higroskopik. Senyawa ini digunakan sebagai pengawet daging dan dalam pembuatan mesiu. -
Senyawa Kalium Iodida dan Kalium Bromida
Kedua garam tersebut terdapat dalam jumlah sedikit di alam (dalam air laut). Keduanya dipakai dalam obat-obatan. KI mempunyai sifat membersihkan darah, sedangkan KBr dapat menenangkan saraf (obat tidur). KBr juga dipakai dalam pemotretan. -
Senyawa Kalium Klorat dan Kalium Hidroksida
Senyawa kalium klorat tidak begitu mudah larut dalam air, merupakan oksidator kuat, lebih-lebih dengan katalis MnO2. Kalium klorat dipakai dalam pembuatan korek api, pembuatan petasan, dan sebagai obat kumur. Adapun kalium hidroksida (KOH) dipakai dalam pembuatan sabun mandi. -
Unsur Litium
Senyawa yang paling penting dari unsur litium adalah senyawa klorida, sulfat, dan karbonat. Litium karbonat digunakan dalam pembuatan peralatan gelas dan keramik. Pada kemurnian yang tinggi senyawa ini digunakan dalam pengobatan pada kerusakan mental tertentu. Senyawa ini juga berfungsi sebagai bahan dalam pembuatan senyawa litium lainnya, misal pada pembuatan litium hidroksida.
Golongan Alkali Tanah
- Unsur Kalsium
Kalsium adalah logam lunak, berwarna putih; mudah bereaksi dengan oksigen, tetapi kalsium oksida yang terbentuk merupakan lapisan yang melindungi logamnya terhadap oksigen lebih lanjut. Kalsium dicampur dengan litium sebagai pengeras dalam logam yang mengandung timbal; untuk industri baja Cr- Ni, kalsium dipakai sebagai campuran logam campur. -
Senyawa Kalsium Sulfat
Senyawa kalsium sulfat (CaSO4) di alam sebagai CaSO4 . 2 H2O yang disebut dengan gips atau albas. Senyawa ini baik digunakan untuk membuat bermacam-macam barang tuang, sebagai pembalut gips, dalam industri cat digunakan sebagai cat “putih”, untuk pembuatan kapur tulis (campuran dari gips, kaolin, asam oleat, dan NaOH). Jika dipanaskan sampai di atas 200 °C, maka air hablurnya lenyap semua (CaSO4 ? 0 H2O). Jika dicampur dengan air kembali maka senyawa tersebut tidak dapat mengikat air lagi. Keadaan demikian dinamakan gips mati. Semen gips dibuat dari gips yang dicampur dengan asam fosfat, Na-fosfat, pasir dan dipanaskan sampai +1200 °C. Hasil ini dicampur lebih lanjut dengan K2SO4 dan ZnSO4, kemudian digiling halus. Semen gips dicampur dengan air dapat menjadi keras dalam waktu 2 jam. -
Unsur Magnesium
Magnesium adalah logam ringan berwarna putih, tetapi dalam udara menjadi putih abu-abu karena terbentuknya lapisan magnesium oksida yang melindungi logamnya terhadap oksidasi lebih lanjut. Dalam bentuk pita atau serbuk magnesium mudah terbakar menjadi magnesium oksida dengan menimbulkan cahaya putih yang menyilaukan. Magnesium dalam asam encer membentuk gas hidrogen. Magnesium dipakai sebagai pengisi lampu Blitzchth (dicampur dengan logam aluminium). Magnesium banyak digunakan untuk pembuatan logam campur, dengan sifatsifat tetap ringan, tetapi dengan kekuatan yang berlipat ganda. Oleh karena itu, magnesium dipakai untuk industri membuat rangka pesawat terbang. -
Senyawa Magnesium Oksida
Magnesium Oksida (MgO) berupa zat padat, berwarna putih, tidak mudah mencair (titik cairnya 2.800 °C), keras dan tahan api. Oleh karena sifat-sifat ini MgO dipakai sebagai pelapis tanur. Jika MgO dipijarkan, dicampur dengan larutan MgCl2 yang pekat, membentuk bubur yang di udara menjadi keras dan mengilap. Campuran tersebut dinamakan semen magnesium atau semen sorel. Campuran semen magnesium dengan serbuk kayu, serbuk gabus, gilingan batu, dan sebagainya disebut granit kayu atau ksilolit. Bahan ini antara lain dipakai untuk membuat lantai yang tidak bersela atau tidak bersambung dan sebagai bahan gading buatan. -
Senyawa Magnesium Sulfat
Magnesium sulfat (MgSO4) berupa padatan putih. Contoh garam inggris dengan rumus MgSO4 ? 7 H2O, dipakai dalam obat-obatan sebagai pencahar (obat urus-urus). -
Senyawa Magnesium Hidroksida
Magnesium Hidroksida (Mg(OH)2) berupa padatan putih yang sedikit larut dalam air. Bersifat basa. Oleh karena itu Mg(OH)2 digunakan untuk obat sakit maag.
Golongan IIIA
- Unsur Aluminium
Aluminium digunakan untuk membuat barang-barang keperluan rumah tangga, misal piring, mangkok, dan sendok; untuk membuat rangka dari mobil dan pesawat terbang; sebagai bahan cat aluminium (serbuk aluminium dengan minyak cat). Aluminium dapat dicairkan menjadi lembaran tipis yang dipakai untuk pembungkus cokelat, rokok dan juga sebagai kaleng minuman bersoda. Daun aluminium atau logam campuran dengan Mg dipakai sebagai pengisi lamput Blitz, di samping gas oksigen. Selanjutnya aluminium dipakai untuk membuat beberapa macam logam campur, diantaranya yang penting ialah duraluminium (paduan 94% aluminium dengan Cu, Mn, Mg), yang terutama dipakai dalam industri pesawat terbang, dan mobil. -
Aluminium Oksida
Aluminium oksida (Al2O3) di alam tercampur dengan oksida besi dalam bentuk hablur yang disebut amaril. Bahan ini sangat keras dan dipakai untuk menggosok besi. Hablur Al2O3 (korundum) juga terdapat dalam bentuk batu permata atau intan berwarna misal mirah berwana merah (mirah delima), nilam berwarna biru (batu nilam), zamrut berwarna hijau, ametis berwarna ungu, ratna cempaka berwarna kuning. Batu-batu ini diperdagangkan dengan nama batu akik, meskipun nama ini tidak tepat karena yang dimaksudkan dengan akik adalah hablur kwarsa (SiO2). -
Senyawa Asam Borat
Asam borat (H3BO3) banyak dipakai dalam pabrik kaca dan email. Pada penyamakan kulit digunakan untuk mengikat kapur dalam kulit. -
Garam-Garam Aluminium Silikat
Beberapa garam aluminium silikat terdapat dalam tanah liat. Tanah liat merupakan bahan dasar dalam pembuatan keramik. Ultramarin adalah bahan cat biru yang terdiri dari Na-Al-silikat dan S. Ultramarin dalam alam terdapat dengan nama lazurit, dipakai sebagai bahan pembiru pakaian, tekstil, kertas, dan gula. -
Senyawa Natrium Perborat
Natrium perborat NaBO3 ? 4 H2O dengan air menimbulkan oksigen aktif yang digunakan sebagai pemucat dalam beberapa macam serbuk sabun.
Silikon
- Unsur Silikon
Oleh karena silikon bersifat semikonduktor sehingga digunakan sebagai bahan baku pada kalkulator, transistor, komputer, dan baterai solar. -
Pasir Kwarsa
Pasir Kwarsa (SiO2) digunakan untuk pembuatan kaca, gelas, porselin, beton. Selain itu SiO2 digunakan untuk menggosok batu kaca, logam-logam untuk pembuatan ampelas dan untuk pembuatan cat tahan udara. -
Kaca Cair Natrium
Kegunaan kaca cair natrium (Na2SiO3) adalah untuk bahan campuran sabun cuci dan perekat dalam pembuatan karton
Golongan VA
- Unsur Nitrogen
Kegunaan nitrogen terutama digunakan dalam pembuatan gas amonia (NH3) dari udara. Gas nitrogen cair digunakan sebagai bahan pembeku dalam industri pengolahan makanan. -
Senyawa Amonia
Kegunaan dari amonia adalah pembuatan es, membuat HNO3, garam-garam amonium, dan sabun amonia. -
Senyawa Asam Nitrat
Asam nitrat digunakan untuk membuat pupuk-pupuk buatan NH4NO3 dan Ca(NO3)2. -
Unsur Fosfor
Fosfor kuning digunakan untuk pembuatan P2O5, yang digunakan untuk mencegah karat dan fosfor merah digunakan untuk membuat kepala batang korek api. Senyawaan fosfor antara lain asam fosfat yang dibuat dengan mereaksikan uap fosfor dengan air. Asam fosfat berguna dalam pembuatan pupuk dan detergen.
Golongan VIA
Unsur Belerang
Belerang digunakan sebagai bahan pembuat asam sulfat, bahan pembuat cat (ultramin, vermilyun, kuning kadmium), pembuat mesiu, untuk membuat karbon disulfida, dan bahan pembuat ebonit. Belerang juga dapat dipakai sebagai obat pemberantas jamur dan untuk memasak getah karet dan getah perca.
Senyawa Belerang Dioksida
Kegunaan belerang dioksida adalah seperti berikut.
- Bahan pengelantang untuk bulu domba, sutra, spons, domen, dan gula tebu.
- Sebagai bahan untuk membersihkan botol-botol dan bejana-bejana anggur.
- Sebagai bahan untuk memberantas penyakit pes di darat dan di kapal-kapal laut.
- Digunakan untuk memurnikan beberapa jenis minyak tanah.
- Senyawa Asam Sulfat
Kegunaan dari asam sulfat antara lain seperti berikut.
- Di laboratorium digunakan untuk pengering dan untuk kimia analisis.
- Dalam teknik industri digunakan sebagai bahan pupuk terutama pupuk fosfat; cat dan pigmen terutama dalam produksi titanium oksida; pembuatan asam (HCl, HNO3, H3PO4).
- Unsur Oksigen
Kegunaan oksigen adalah untuk membantu pernapasan pasien (dalam kedokteran) dan untuk isi tabung udara yang dibawa penyelam. Salah satu senyawaan oksigen adalah ozon (O3). Ozon dibuat dari O2 yang dialirkan melalui pesawat pengozon. Di dalam pesawat ini terjadi letusan-letusan listrik yang menyebabkan O2 berubah menjadi O3. Kegunaan ozon adalah sebagai pemucat benang dan bahan pemusnah hama air minum.
Golongan VIIA atau Halogen
- Unsur Klor
Klor digunakan dalam industri kertas dan industri tekstil sebagai pengelantang, sebagai pemusnah kuman, dan untuk pembuatan kapur klor, brom, dan zat warna organik. -
Senyawa Asam Klorida
Asam klorida (HCl) digunakan untuk membersihkan logamlogam dan untuk membuat garam-garam klorida dan gas klor. HCl murni yang tidak mengandung air banyak digunakan dalam pembuatan zat warna organik. -
Garam Hipoklorit dan Garam Klorat
Garam klorat yang penting adalah kalium klorat (KClO3) yang digunakan untuk kepala batang korek api, petasan, dan dipakai sebagai obat kumur. -
Unsur Brom
Larutan brom dalam air (aqua bromata) digunakan sebagai pengoksidasi. Kurang lebih 90% brom dipakai sebagai bahan membuat garam-garam bromida. AgBr dipergunakan dalam pemotretan. NaBr dan KBr dipergunakan dalam obat-obatan. Beberapa garam bromida lainnya digunakan dalam pembuatan zat-zat warna. -
Unsur Iod
Larutan iod dalam alkohol dinamakan iodtinktur dan digunakan sebagai pemusnah hama. Iod juga mudah larut dalam karbon disulfida dan kloroform. Iod digunakan dalam obat-obatan sebagai kalium iodida (KI) dan iodoform (CHI3). -
Senyawa Asam Fluorida
Dalam bentuk cair atau gas, HF dapat memakan kaca yang dinamakan mengets menurut reaksi seperti berikut.
Asam fluorida digunakan untuk pemucatan penjalin. Adapun senyawa-senyawa organik fluor digunakan untuk pendingin dalam lemari es dan untuk mematikan kutu-kutu dalam kain.
Golongan VIIIA atau Gas Mulia
- Helium (He) sudah dikenal lebih dahulu daripada gas-gas mulia lainnya. Untuk pertama kali helium ditemukan di dalam atmosfer matahari. Helium digunakan untuk mengisi balon. Helium memiliki berat dua kali lebih berat daripada hidrogen, tetapi tidak dapat terbakar.
-
Argon dicampur dengan nitrogen digunakan sebagai pengisi lampu pijar dan lampu-lampu radio untuk menahan mengabutnya kawat wolfram dalam lampu itu.
-
Neon (Ne) dipakai sebagai pengisi lampu-lampu neon yang memberikan cahaya merah. Jika dicampur dengan uap raksa akan memberikan cahaya putih kebiru-kebiruan jika tabung kacanya tidak berwarna, atau cahaya hijau jika tabung kacanya berwarna cokelat.
-
Kripton (Kr) dan xenon (Xe) akhir-akir ini diketemukan bahwa xenon bersifat anestesi. Oleh karena sifat ini maka xenon digunakan untuk membius pasien-pasien dalam operasi besar. Akan tetapi pemakaian ini masih terlalu mahal.
Baca Juga Artikel Yang Mungkin Berhubungan : Pengertian Kimia – Sejarah, Cabang, Konsep, Industri, Manfaat
Dampak Negatif Unsur dan Senyawa
Selain bermanfaat ternyata unsur-unsur yang telah kita pelajari mempunyai dampak negatif. Adapun dampak negatifnya adalah seperti berikut.
- Karbon
Dampak negatif karbon adalah pada senyawa karbon yaitu:
a. Karbon dioksida (CO2) Karbon dioksida terjadi pemakaian bahan bakar dari fosil. Adanya pembakaran ini menyebabkan terjadinya efek rumah kaca.
b. Cloro Fluoro Carbon (CFC) CFC berdampak negatif terhadap penipisan lapisan ozon dan berkontribusi terhadap efek rumah kaca.
c. Kloroform (CCl4) Kloroform menyebabkan kerusakan hati dan ginjal, dan bersifat racun bila tertelan.
d. Karbon disulfida (CS2) Karbon disulfida merupakan senyawa mudah terbakar dan bersifat meracuni.
e. Karbon monoksida (CO) Karbon monoksida biasanya dihasilkan oleh asap kendaraan dan proses industri. Karbon monoksida lebih mudah mengikat hemoglobin daripada oksigen. Oleh karena itu, darah akan kekurangan oksigen. -
Nitrogen
Campuran NO dan NO2 menghasilkan NOx yang merupakan hasil pembakaran bahan bakar dari industri atau kendaraan yang menyebabkan terjadinya hujan asam dan asap kabut (smog) yang mengakibatkan terjadinya iritasi pada mata dan menyebabkan tumbuhan menjadi kering. Hujan asam dapat merusak pH tanah, perairan serta merusakkan bangunan. -
Silikon
Silikon yang dipakai untuk kecantikan wajah dapat menyebabkan kerusakan bentuk dan melumpuhkan beberapa otot wajah. Hal ini karena silikon dapat membentuk gumpalan dan dapat memblokir aliran darah ke jaringan/organ tubuh. -
Fosfor
Fosfor berdampak negatif apabila bijih fosfor yang diolah menjadi fosfat larut dalam air, sehingga menyebabkan terjadinya limbah radioaktif (disebabkan bijih fosfor mengandung uranium). -
Belerang
Senyawa belerang yang berdampak negatif antara lain:
a. Hidrogen Sulfida (H2S)
b. Hidrogen sulfida gas sangat beracun yang bau seperti telur busuk dan senyawa ini menyebabkan kematian.
c. Asam Sulfat (H2SO4)
d. Asam sulfat merupakan zat higroskopis sehingga dapat merusak kulit dan juga menyebabkan korosi. -
Radon
Radon merupakan unsur gas mulia yang bersifat radioaktif. Radon apabila terhirup oleh manusia, akan tertinggal di paruparu dan menimbulkan kanker paru-paru. -
Aluminium
Aluminium dapat merusak kulit dan dalam bentuk bubuk dapat meledak di udara bila dipanaskan. Senyawa aluminium yang berbahaya antara lain aluminium oksida (Al2O3) yang bereaksi dengan karbon dan berdampak pada pemanasan global.
Daftar Pustaka
Sukmanawati, Wening, 2009, Kimia untuk SMA dan MA kelas XII, Jakarta : Pusat perbukuan Departemen Pendidikan Nasional