Perubahan Wujud Zat
Dalam ilmu fisika setiap segala sesuatu yang mempunyai massa dan yang menempati suatu ruang disebut dengan zat. Dan jika yang tidak mempunyai massa namun menempati ruang maka termasuk tergolong kedalam sebuah energi. Yang termasuk yang tidak memiliki massa seperti bunyi dan cahaya. Jadi, dalam ilmu fisika bahwa sesungguhnya ilmu yang menyangkut mengenai zat dan energi. Namun kali ini diulas tentang masalah wujud zat dan perubahannya, wujud zat dapat berubah karena adanya kalor yang diberikan atau dilepaskan.
Perubahan wujud zat adalah perubahan termodinamika dari satu fase benda ke keadaan wujud zat yang lain. Perubahan wujud zat ini bisa terjadi karena peristiwa pelepasan dan penyerapan kalor.Perubahan wujud zat terjadi ketika titik tertentu tercapai oleh atam/senyawa zat tersebut yang biasanya dikuantitaskan dalam angka suhu. Semisal air untuk menjadi padat harus mencapai titik bekunya dan air menjadi gas harus mencapai titik didihnya.
Berikut adalah Perubahan wujud zat :
Didalam ilmu fisika teori dasar zat terbagi menjadi 3 wujud yaitu :
- Zat padat
- Zat cair
- Dan Zat gas
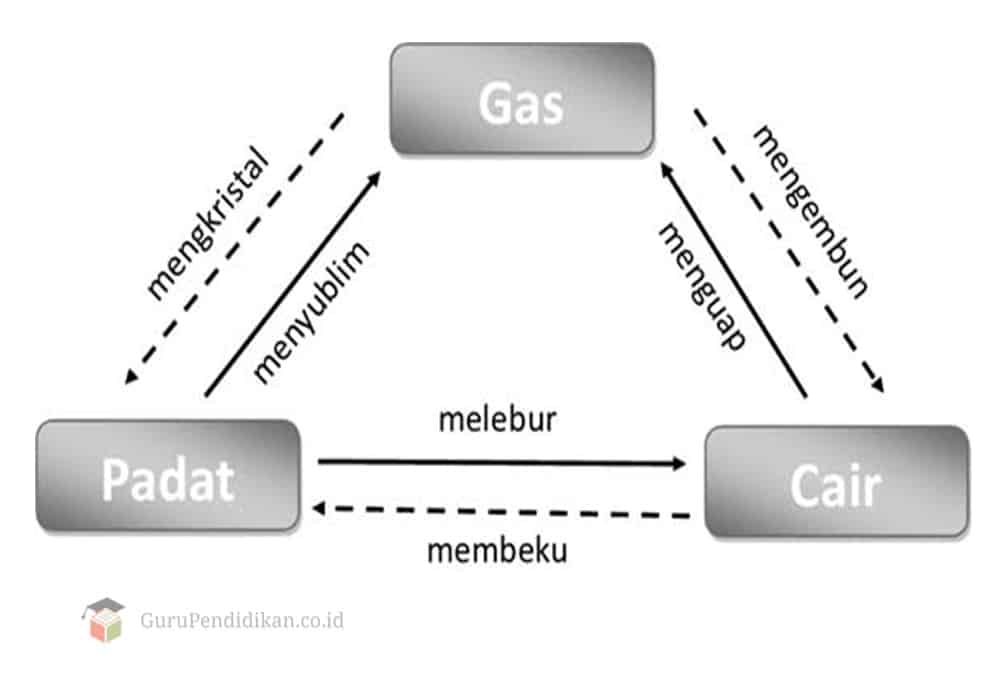
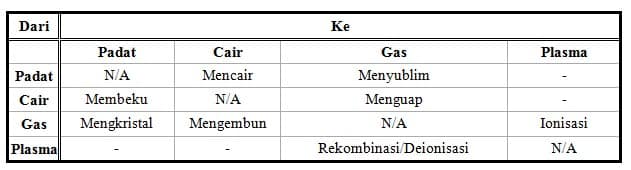
Di dalam pelajaran ilmu IPA fisika teori dasar mengenai zat tersebut menjelasakan bahwa zat bisa mengalami suatu perubahan wujud. Pada zat padat dapat yang mengalami perubahan wujud menjadi zat cair hal ini biasa disebut dengan melebur. Yang diantaranya seperti bungkahan, es dapat berubah menjadi air. Kemudian air dapat berubah menjadi uap yang disebut dengan peristiwa menguap. Yang diantaranya seperti peristiwa menguapnya air dipermukaan bumi menjadi uap air di awan. Kebalikan perubahan wujud diatas ialah mengembun dan membeku. Terjadinya kondisi uap air di angkasa bisa mengalami peristiwa terjadinya pengembunan hal ini karena adanya embun tersebut yang menempel/melekat pada benda atau tumbuhan apa saja dipagi hari.
Ada juga peristiwa perubahan wujud yang tidak mengalami proses terjadinya melebur melainkan langsung menjadi uap, peristiwa ini disebut dengan menyublin diantaranya seperti kapur barus berubah langsung menjadi uap. Proses sebaliknya disebut dengan mengkristal yang dimana upa kapur barus dapat berubah wujud menjadi kristal kapur barus.
Baca Juga Artikel Yang Mungkin Berhubungan : √ Pengertian Dan Ciri Zat Padat, Gas, Cair Beserta Contohnya
Pengertian Kalor
Q = mc∆T ………. Pers. (1)
Keterangan:
- Q = jumlah kalor yang diberikan (kalori atau joule)
- m = massa benda (g atau kg)
- c = kalor jenis (kal/goC atau J/kgoC)
- ∆T = perubahan suhu (oC)
Baca Juga Artikel Yang Mungkin Berhubungan : Apa Itu Perubahan Wujud Zat Dan Jenis Beserta Contohnya
Kalor dan Perubahan Wujud
Dibagian atas bab ini sudah dijelaskan bahwa kalor adalah energi yang berpindah dari benda yang bersuhu lebih tinggi ke benda yang bersuhu lebih rendah jika benda tersebut saling bersentuhan. Kalor dapat diukur dengan menggunakan calorimeter, tetapi seringkali calorimeter digunakan untuk menentukan kalor jenis suatu zat dengan cara mencampurkan zat tersebut ke dalam calorimeter bersama zat yang massa jenisnya sudah diketahui.
Dapat dirumuskan seperti dibawah ini :
Q = mct. 4t
Keterangan :
- Q = Kalor (joule)
- C = Kalor Jenis (j/kg.K)
- 4t = Perubahan suhu (c)
Kalor jenis adalah kalor yang diperlukan untuk menaikkan suhu 1 kg suatu zat sebesar 1c atau 1K. Berdasarkan definisi diatas kalor jenis merupakan kemampuan khas suatu zat untuk menyerap kalor.
-
Kapasitas Kalor
Kapasitas kalor (c) adalah banyaknya energi yang harus diberikan dan berbentuk kalor pada suatu zat untuk menaikkan suhu. Zat tersebut sebesar 1 derajat. Kapasitas kalor dapat dirumuskan seperti dibawah ini :
C = 4Q/4t
c = Kapasitas kalor (j/kg)
Keterangan :
- Q = Kalor (joule)
- c = Kalor jenis zat (j/kg)
- 4t = Perubahan suhu (c)
-
Perubahan Wujud
Sebingkah es dengan suhu minus beberapa derajat celcius diberikan kalor sehingga suhu naik mencapai 0˚C beberapa lama sampai suhu tersebut .
Tidak naik lagi maka suhunya kembali naik sehingga mencapai 100˚C. Besar kalor yang dibutuhkan dalam proses tersebut yaitu :
Q total = Q1 + Q2 + Q3 + Q4
Keterangan :
- Q1 = dihitung ketika semua masih berbentuk es
- Q2 = erupakan nilai kalor yang dibutuhkan untuk melebur semua es
- Q3 = kalor yang dibutuhkan untuk menaikkan suhu air dari 0˚C sampai 100˚ C
- Q4 = kalor yang dibutuhkan untuk mengubah air menjadi air
Baca Juga Artikel Yang Mungkin Berhubungan : Pengertian Dan Macam Klasifikasi Zat
Pengaruh Kalor Terhadap Wujud Zat
Kalor bisa menaikkan suhu suatu zat yang berdampak terhadap terjadinya perubahan wujud zat. Melebur dan menguap yang merupakann peristiwa yang membutuhkan kalor, karena untuk dapat meleburkan sebuah bungkahan es ataupun untuk menguapkan air dibutuhkan kalor.
Numun peristiwa mengembun dan membeku tidak membutuhkan kalor melainkan melepaskannya, peristiwa terjadinya terbentuknya embun dipagi hari merupakan contoh dari perubahan wujud yang melepaskan kalor. Begitu juga peristiwa membeku akan dikeluarkan sejumlah kalor sehingga air membeku membentuk bungkahan es.
Seperti kulkas ( lemari es ) merupakan penerapan peristiwa terjadinya perubahan wujud zat cair yang menjadi padat, alat difungsikan untuk mengeluarkan kalor yang ada pada air. Jadi deemikian bungkahan es dapat terbentuk dikulkas karena kalor pada air telah dikeluarkan oleh alat tersebut.
Jadi bisa disimpulkan bahwa zat yang mengalami perubahan zat disebabkan adanya kalor, dalam proses yang demikian kalor itu dibutuhkan oleh zat untuk mengubah wujudnya, namun ada pula yang tidak membutuhkan kalor alias dilepaskan.
Baca Juga Artikel Yang Mungkin Berhubungan : Perbedaan Metanol Dan Bensin – Pengertian, Sejarah, Produksi, Kegunaan, Karakteristik, Cara Kerja, Zat Pencemaran
Contoh Soal dan Pembahasan
Soal Pertama
- m = 3 kg
- ∆T = 80oC – 10oC = 70oC
- cbesi = 450 J/kgoC
- Q = mc∆T
- Q = 3 × 450 × 70
- Q = 9,45 × 104 J
- = 94,5 kJ
Soal Kedua
- mes = 0,5 kg
- Tes = -5oC
- Cces = 2.100 J/kgoC
- mair = 1 kg
- Tair = 20
- ccair = 4.200 J/kg C
- Qair = Qes
- mair × cair × (Tair –TC) = mes × ces × (TC – Tes)
- 1 × 4.200 × (20 – TC) = 0,5 × 2.100 × (TC – (-5)
- 4.200 × (20 – TC) = 1.050 (TC + 5)
- 4 × (20 – TC) = (TC + 5) → kedua ruas dibagi 1.050
- 80 – 4TC = TC + 5
- TC + 4TC = 80 – 5
- 5TC = 75
- TC = 75/5
- TC = 15
Soal Ketiga
- mAg = 16,5 kg (Ag = Agentum, nama ilmiah perak)
- LB = 88 kJ/kg = 8,8 × 104 J/kg
- TAg = 20oC
- Titik lebur perak (TL) = 961oC
- cAg = 230 J/kgoC
- Cara pertama adalah mencari kalor untuk menaikkan suhu hingga mencapai titik didihnya.
- Cara kedua adalah mencari kalor leburnya.
- Q1 = mc∆T
- Q1 = 16,5 × 230 × (961 – 20)
- Q1 = 3,61 × 106 J
- Q2 = mLB
- Q2 = 16,5 × (8,8 × 104)
- Q2 = 1,452 × 106 J
- Qtot = Q1 + Q2
- Qtot = (3,61 × 106) + (1,452 × 106)
- Qtot = 5,062 × 106 J
Soal Keempat
- ma = 100 g = 0,1 kg
- Ta = 40oC
- Ca = 1 kkal/kg
- LB-es = 0,5 kkal/kg
- Qair = Qes
- maca∆T = mesLB
- 0,1 × 1 × (40 – 0) = mes × 0,5
- 0,5mes = 4
- mes = 4/0,5
- mes = 8 kg