Perbedaan Metanol Dan Bensin – Pengertian, Sejarah, Produksi, Kegunaan, Karakteristik, Cara Kerja, Zat Pencemaran : Mungkin tidak dapat menemukan benisn biasa atau mungkin tergantung selera anda masing-masing yang untuk hal demikian ini yang penting jangan sampai salah dalam memilih dan dapat meningkatkan kinerja dan efisiensi bahan bakar dari kendaraan anda.
Pengertian Metanol
Metanol merupakan salah satu jenis bahan bakar alternatif untuk mesin pembakaran dalam dan beberapa jenis mesin yang lainnya. Metanol dapat digunakan dengan mencampurkannya dengan bensin atau dipakai sendirian “metanol murni”, di Amerika Serikat, bahan bakar metanol mendapatkan perhatian yang lebih kecil dari pada bahan bakar etanol, karena dukungan untuk etanol sendiri yang dibuat dari jagung dapat memunculkan beberapa keuntungan politik.
Baca Juga Artikel Yang Mungkin Berhubungan : Pengertian Suhu Beserta Perubahan Dan ALat Ukurnya
Secara umum, etanol juga lebih tidak beracun dan mempunyai kandungan energi yang lebih tinggi, meskipun sebenarnya metanol lebih murah untuk diproduksi dan membutuhkan dana lebih sedikit untuk mengurangi emisi karbonya.
Walaupun begitu, untuk mengoptimalkan performa mesin, kesediaan bahan bakar, keuntungan politis dan kesehatan, campuran dari etanol, metanol dan bensin sebaiknya digunakan bersamaan dari pada hanya menggunakan ketiga jenis bahan bakar ini secara terpisah. Metanol dapat dibuat dari fosil atau sumber energi terbaharui lainnya.
Sejarah Metanol
Dalam proses pengawetan mayat, orang Mesir kuno menggunakan berbagai macam campuran, termasuk di dalamnya metanol, yang mereka peroleh dari pirolisis kayu. Methanol murni, pertama kali berhasil diisolasi tahun 1661 oleh Robert Boyle, yang menamakannya spirit of box, karena ia menghasilkannya melalui distilasi kotak kayu. Nama itu kemudian lebih dikenal sebagai pyroxylic spirit (spiritus).
Pada tahun 1834, ahli kimia Perancis Jean-Baptiste Dumas dan Eugene Peligot menentukan komposisi kimianya. Mereka juga memperkenalkan namamethylene untuk kimia organik, yang diambil dari bahasa Yunani methy = “anggur”) + hŷlē =kayu (bagian dari pohon). Kata itu semula dimaksudkan untuk menyatakan “alkohol dari (bahan) kayu”, tetapi mereka melakukan kesalahan.
Kata methyl pada tahun 1840 diambil dari methylene, dan kemudian digunakan untuk mendeskripsikan “metil alkohol”. Nama ini kemudian disingkat menjadi “metanol” tahun 1892 oleh International Conference on Chemical Nomenclature. Suffiks [-yl] (indonesia {il}) yang digunakan dalam kimia organik untuk membentuk nama radikal-radikal, diambil dari kata “methyl”.
Pada tahun 1923, ahli kimia Jerman, Matthias Pier, yang bekerja untuk BASF mengembangkan cara mengubah gas sintesis (syngas / campuran dari karbon dioksida and hidrogen) menjadi metanol. Proses ini menggunakan katalis zinc chromate (seng kromat), dan memerlukan kondisi ekstrem —tekanan sekitar 30–100 MPa (300–1000 atm), dan temperatur sekitar 400 °C. Produksi metanol modern telah lebih effisien dengan menggunakan katalis tembaga yang mampu beroperasi pada tekanan relatif lebih rendah.
Baca Juga Artikel Yang Mungkin Berhubungan : Pengertian Larutan Dan Kelarutan Dalam Kimia Beserta Contohnya
Penggunaan metanol sebagai bahan bakar mulai mendapat perhatian ketika krisis minyak bumiterjadi di tahun 1970-an karena ia mudah tersedia dan murah. Masalah timbul pada pengembangan awalnya untuk campuran metanol-bensin. Untuk menghasilkan harga yang lebih murah, beberapa produsen cenderung mencampur metanol lebih banyak.
Produsen lainnya menggunakan teknik pencampuran dan penanganan yang tidak tepat. Akibatnya, hal ini menurunkan mutu bahan bakar yang dihasilkan. Akan tetapi, metanol masih menarik utuk digunakan sebagai bahan bakar bersih. Mobil-mobil dengan bahan bakar fleksibel yang dikeluarkan oleh General Motors, Ford dan Chrysler dapat beroperasi dengan setiap kombinasi etanol, metanol dan/atau bensin.
Produksi Metanol
Saat ini, gas sintesis umumnya dihasilkan dari metana yang merupakan komponen dari gas alam. Terdapat tiga proses yang dipraktekkan secara komersial. Pada tekanan sedang 1 hingga 2 MPa (10–20 atm) dan temperatur tinggi (sekitar 850 °C), metana bereaksi dengan uap air (steam) dengan katalis nikel untuk menghasilkan gas sintesis menurut reaksi kimia berikut:
CH4 + H2O → CO + 3 H2
Reaksi ini, umumnya dinamakan steam-methane reforming atau SMR, merupakan reaksi endotermik dan limitasi perpindahan panasnya menjadi batasan dari ukuran reaktor katalitik yang digunakan. Metana juga dapat mengalami oksidasi parsial dengan molekul oksigen untuk menghasilkan gas sintesis melalui reaksi kimia berikut:
2 CH4 + O2 → 2 CO + 4 H2
reaksi ini adalah eksotermik dan panas yang dihasilkan dapat digunakan secara in-situ untuk menggerakkan reaksi steam-methane reforming. Ketika dua proses tersebut dikombinasikan, proses ini disebut sebagai autothermal reforming. Rasio CO and H2 dapat diatur dengan menggunakan reaksi perpindahan air-gas (the water-gas shift reaction):
CO + H2O → CO2 + H2,
untuk menghasilkan stoikiometri yang sesuai dalam sintesis metanol.
Karbon monoksida dan hidrogen kemudian bereaksi dengan katalis kedua untuk menghasilkan metanol. Saat ini, katalis yang umum digunakan adalah campuran tembaga, seng oksida, dan alumina, yang pertama kali digunakan oleh ICI di tahun 1966. Pada 5–10 MPa (50–100 atm) dan 250 °C, ia dapat mengkatalisis produksi metanol dari karbon monoksida dan hidrogen dengan selektifitas yang tinggi:
Baca Juga Artikel Yang Mungkin Berhubungan : Pengertian Pengendalian Proses Teknik Kimia Beserta Tipe Dan Contohnya
CO + 2 H2 → CH3OH
Sangat perlu diperhatikan bahwa setiap produksi gas sintesis dari metana menghasilkan 3 mol hidrogen untuk setiap mol karbon monoksida, sedangkan sintesis metanol hanya memerlukan 2 mol hidrogen untuk setiap mol karbon monoksida. Salah satu cara mengatasi kelebihan hidrogen ini adalah dengan menginjeksikan karbon dioksida ke dalam reaktor sintesis metanol, dimana ia akan bereaksi membentuk metanol sesuai dengan reaksi kimia berikut:
CO2 + 3 H2 → CH3OH + H2O
Walaupun gas alam merupakan bahan yang paling ekonomis dan umum digunakan untuk menghasilkan metanol, bahan baku lain juga dapat digunakan. Ketika tidak terdapat gas alam, produk petroleum ringan juga dapat digunakan. Di Afrika Selatan, sebuah perusahaan (Sasol) menghasilkan metanol dengan menggunakan gas sintesis dari batu bara.
Kegunaan Metanol
Berikut Ini Merupakan Kegunaan Metanol.
Bahan Bakar Ontuk Kendaraan Bermotor
Metanol digunakan secara terbatas dalam mesin pembakaran dalam, dikarenakan metanol tidak mudah terbakar dibandingkan denganbensin. Metanol juag digunakan sebagai campuran utama untuk bahan bakar model radio kontrol, jalur kontrol, dan pesawat model.
Salah satu kelemahan metanol jika digunakan dalam konsentrasi tinggi adalah sifat korosif terhadap beberapa logam, termasuk aluminium. Metanol, meskipun merupakan asam lemah, menyerang lapisan oksida yang biasanya melindungi aluminium dari korosi:
6 CH3OH + Al2O3 → 2 Al(OCH3)3 + 3 H2O
Ketika diproduksi dari kayu atau bahan oganik lainnya, metanol organik tersebut merupakan bahan bakar terbaharui yang dapat menggantikan hidrokarbon. Namun mobil modern pun masih tidak bisa menggunakan BA100 (100% bioalkohol) sebagai bahan bakar tanpa modifikasi. Metanol juga digunakan sebagai pelarut dan sebagai antibeku, dan fluida pencuci kaca depan mobil.
Baca Juga Artikel Yang Mungkin Berhubungan : Pengertian Magma, Lava Dan Lahar Pada Gunung Berapi
Bahan Utama Untuk Bahan Lain
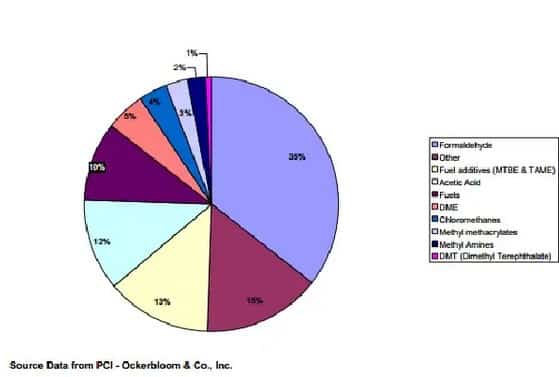
Penggunaan metanol terbanyak adalah sebagai bahan pembuat bahan kimia lainnya. Sekitar 40% metanol yang ada diubah menjadi formaldehid, dan dari sana akan dihasilkan berbagai macam produk seperti plastik, plywood, cat, peledak, dan tekstil.
Senyawa kimia lainnya yang merupakan turunan dari metanol adalah dimetil eter, yang telah menggantikan klorofluorokarbon sebagai bahan campuran pada aerosol, dan asam asetat. Dimetil eter juga dapat dicampur dengan gas alam terkompresi (LPG) untuk memanaskan masakan, dan juga bisa digunakan sebagai bahan bakar pengganti diesel.
Dalam beberapa pabrik pengolahan air limbah, sejumlah kecil metanol digunakan ke air limbah sebagai bahan makanan karbon untukdenitrifikasi bakteri, yang mengubah nitrat menjadi nitrogen.
bahan bakar direct-metanol unik karena suhunya yang rendah, operasi pada tekanan atmofser, mengijinkan mereka dibuat kecil. Ditambah lagi dengan penyimpanan dan penanganan yang mudah dan aman membuat metanol dapat digunakan dalam perlengkapan elektronik.
Pengertian Bensin
Bensin “gasoline” atau “petrol” merupakan salah satu jenis bahan bakar minyak yang dimaksudkan untuk kendaraan bermotor roda dua, tiga dan empat, yang secara sederhana, bensin tersusun dari hidrokarbon rantai lurus, mulai dari C7 “heptana” hingga dengan C11, dengan kata lain,
bensin terbuat dari molekul yang hanya terdiri dari hidrogen dan karbon yang terikat antara satu dengan yang lainnya yang dalam hal ini sehingga membentuk rantai. Bila bensin dibakar pada kondisi ideal dengan oksigen berlimpah, maka akan dihasilkan CO2, H2O dan energi panas. Yang setiap kg bensin mengandung 42.4 MJ.
Bensin dibuat dari minyak mentah, cairan berwarna hitam yang dipompa dari perut bumi dan biasa disebut dengan petroleum. Cairan ini mengandung hidrokarbon, atom-atom karbon dalam minyak mentah ini berhubungan satu dengan yang lainnya dengan cara membentuk rantai yang panjangnya yang berbeda-beda.
Molekul hidrokarbon dengan memiliki panjang yang berbeda akan memiliki sifat yang berbeda pula. CH4 “metana” merupakan molekul paling “ringan” dengan bertambahnya ataom C dalam rantai tersebut akan membuatnya semakin “berat”.
Empat molekul pertama hidrokarbon ialah metana, etana, propana, dan butana. Yang dalam temperatur dan tekanan kamar, yang keempatnya berwujud gas, dengan titik didih masing-masing -107, -67, -43 dan -18 derajat celcius. Berikutnya dari C5 hingga dengan C18 berwujud cair dan mulai dari C19 ke atas yang berwujud padat.
Yang dengan bertambah panjangnya rantai hidrokarbon akan menaikkan titik didihnya, yang sehingga pemisahan hidrokarbon ini dilakukan dengan cara distilasi, prinsip inilah yang diterapkan di pengilangan minyak untuk memisahkan berbagai fraksi hidrokarbon dari minyak mentah.
Baca Juga Artikel Yang Mungkin Berhubungan : Definisi Komponen Biotik Dalam Ekosistem Dan Contohnya
Karakteristik Bensin
- Mudah menguap pada temperatur normal.
- Tidak berwarna, tembus pandang, dan berbau.
- Mempunyai titik nyala rendah (-10 sampai -15 derajat Celcius).
- Mempunyai berat jenis yg rendah (0,71 sampai 0,77 kg/l).[4]
- Dapat melarutkan oli dan karet.
- Menghasilkan jumlah panas yang besar (9,500 sampai 10,500 kcal/kg).
- Sedikit meninggalkan jelaga setelah dibakar.
Cara Kerja Bensin Dalam Mesin
Bensin bekerja di dalam mesin pembakaran yang ditemukan oleh Nikolaus Otto. Mesin pembakaran dikenal pula dengan nama Mesin Otto. Cara kerja bensin di dalam mesin pembakaran:
- Bensin dari tangki masuk ke dalam karburator. Kemudian bercampur dengan udara. Pada mesin modern, peran karburator digantikan oleh sistem injeksi. Sebuah sistem pembakaran baru yang bisa meminimalisiremisi gas buang kendaraan.
- Campuran bensin dan udara kemudian dimasukkan ke dalam ruang bakar.
-
Selanjutnya, campuran bensin dan udara yang sudah berbentuk gas, ditekan oleh piston hingga mencapai volume yang sangat kecil.
- Gas ini kemudian dibakar oleh percikan api dari busi.
- Hasil pembakaran inilah yang menghasilkan tenaga untuk menggerakkan kendaraan.
Dalam kenyataannya, pembakaran gas di dalam mesin tidak berjalan dengan sempurna. Salah satu masalah yang sering muncul adalah “ketukan di dalam mesin”, atau disebut sebagai “mesin ngelitik” atau knocking. Jika dibiarkan, knocking dapat menyebabkan kerusakan pada mesin. Knocking terjadi karena campuran udara dan bahan bakar terbakar secara spontan karena tekanan tinggi di dalam mesin, bukan karena percikan api dari busi.
Baca Juga Artikel Yang Mungkin Berhubungan : Pengertian Elektrolit Dan Non Elektrolit Beserta Contohnya
Zat Pencemaran Hasil Pembakaran BBM
Pembakaran bensin dalam mesin kendaraan mengakibatkan pelepasan berbagai zat yang dapat mengakibatkan pencemran udara.
- CO2
- CO dari pembakaran bahan bakar yang tidak sempurna, bersifat racun.
- NOx(NO, NO2). Pembakaran bahan bakar dalam suhu yang tinggi di mana nitrogen dalam udara ikut teroksidasi. NOx dapat menyebabkan hujan asam dan smog fotokimia
- Pb pada penggunaan bensin yang mengandung aditif senyawa timbal bersifat racun
Bensin yang digunakan oleh kendaraan akan menimbulkan dua masalah utama. Masalah pertama adalah asap dan ozon di kota-kota besar. Masalah kedua adalah karbon dan gas rumah kaca.
Idealnya, ketika bensin dibakar di dalam mesin kendaraan, akan menghasilkan CO2dan H2O saja. Kenyataannya pembakaran di dalam mesin tidaklah sempurna, dalam proses pembakaran bensin, dihasilkan juga:
-
- Karbon monoksida, CO, yang merupakan gas beracun.
- Nitrogen oksida, NOx, sebagai sumber utama asap di perkotaan yang jumlah kendaraannya sangat banyak.
- Hidrokarbon yang tidak terbakar.
Oleh karena alasan-alasan inilah, para ilmuwan sekarang sedang berusaha untuk mengganti bahan bakar bensin dengan bahan bakar hidrogen yang lebih ramah lingkungan, karena jika H2 ini direaksikan dengan O2 hanya akan menghasilkan uap air.
Perbedaan Antara Metanol Dan Bensin
Ada beberapa perbedaan antara metanol dan bensin yang diantaranya yaitu:
- Metanol ialah bio-fuel masa depan, sedangkan bensin tidak ramah lingkungan.
- Bensin dan metanol keduanya digunakan sebagai bahan bakar mobil dan metanol lebih kuat dari pada bensin.
- Methanol mahal dan digunakan sebagai bahan bakar pengganti dibandingkan dengan bensin.
- Bensin dan metanol keduanya beracun dan kontak dengan kulit harus dihindari terutama dalam kasus metanol.
Metanol kurang mudah terbakar dari pada bensin tetapi dapat menimbulkan korosi pada bagian logam di mesin.
Baca Juga Artikel Yang Mungkin Berhubungan : Penjelasan Air Sebagai Pelarut Bagi Kehidupan