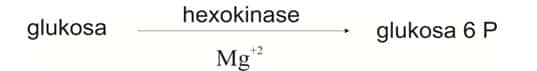Pengertian Koenzim, Fungsi, Komponen, Struktur, Perbedaan dan Klasifikasi adalah sebuah zat yang bekerja dengan enzim untuk memulai atau membantu fungsi enzim. Koenzim ini tidak bisa berfungsi sendiri dan membutuhkan kehadiran enzim
Baca Juga Artikel Yang Mungkin Berhubungan : “Katalis ( Katalisator ) Pengertian & ( Fungsi – Contoh ) Serta Sifat Enzim Sebagai Biokatalisator
Pengertian Koenzim
Pengertian Koenzim ialah sebuah zat yang bekerja dengan enzim untuk memulai atau membantu fungsi enzim. Koenzim ini tidak bisa berfungsi sendiri dan membutuhkan kehadiran enzim. Sebuah non-protein organik yang memainkan peran penting dalam beberapa reaksi yang dikatalisis oleh enzim itu sendiri.
Koenzim adalah ko-faktor yang berupa molekul organik kecil yang merupakan bagian enzim yang tahan panas, mengandung ribose dan fosfat, larut dalam air dan bisa bersatu dengan apoenzim membentuk holoenzim. Koenzim yang membentuk ikatan sangat erat baik secara kovalen maupun non kovalen dengan apoenzim di sebut gugus prostetik. Koenzim memiliki fungsi aktif sebagai katalisator yang dapat meningkatkan kemampuan katalitik suatu enzim. Selain itu koenzim juga berfungsi untuk menentukan sifat dari suatu reaksi dan dapat bertindak sebagai transpor elektron dari satu enzim ke enzim yang lain. Contoh koenzim adalah NADH, NADP dan adenosin trifosfat.
Koenzim merupakan komponen penting dari enzim yang diperlukan untuk setiap reaksi metabolisme dalam tubuh kita. Koenzim sering di identikan sebagai vitamin karena banyak koenzim ditemukan dalam bentuk derivat vitamin B seperti Niacin, Tiamin, Riboflavin, dl. Koenzim berikatan dengan enzim membentuk holoenzim. Koenzim juga membentuk molekul lain dalam sel yang menjadi sumber energi Sel. Energi sell dibutuhkan molekul-molekul sel untuk melakukan fungsi-fungsi khusus. Contoh dari salah satu fungsi koenzim bagi tubuh adalah retensi memori. Tanpa koenzim, tubuh manusia tidak bekerja dan semua proses sel berhenti.
Baca Juga Artikel Yang Mungkin Berhubungan : Enzim – Pengertian, Cara, Sifat, Faktor, Penamaan, Persyaratan, Contoh
Koenzim dan Vitamin
- Kofaktor dibutuhkan oleh apoenzim inaktif (hanya protein) untuk diubah menjadi holoenzim aktif.
- Ada dua jenis kofaktor yaiu ion esensial (biasanya ion logam) dan komponen organi yang biasa disebut koenzim. Keduanya memiliki kegunaan yang sama pada sisi aktif pada enzim yang bersangkutan.
- Mineral merupakan kofaktor. Beberapa ion esensial merupakan ion aktivator yang terikat secara reversibel dan sering terlibat dalam pengikatan substrat sedangkan kation (metaloenzim) terikat kuat dan hanya kadang-kadang saja terlibat secara langsung dalam reaksi katalisis
- Koenzim bereaksi sebagai reagen gugus traansfer yang spesifik pada gugus kima yang dapat menerima dan mendonor. Beberapa koenzim, gugus hidrogen atau sebuah elektron, beberapa koenzim dapat mengangkut lebih banyak dan terikat secara kovalen dengan gugus kimia.
- Gugus metabolit terikat pada pusat rektif dari koenzim
- Pada mamalia terdapat koenzim yang merupakan turunan dari prekursor makanan yang disebut vitamin.
Baca Juga Artikel Yang Mungkin Berhubungan : Pengertian Enzim Pepsin Beserta Cara Kerjanya
Klasififikasi Koenzim
- Diklasifikasikan menjadi 2 tipe berdasarkan interaksi dengan apoenzim yaitu kosubstrat dan gugus prostetik.
- Kosubstrat adalah substrat pada enzim yang mengkatalisis reaksi dengan cara mengubah jalan reaksi dan mendisosiasi sisi aktif. Struktur awal dari kosubstrat diregenerasi oleh reaksi lanjutan yang dikatalisis oleh enzim lain. Kosbstrat dapat didaur ulang berkali-kali didalam sel, tidak seperti substrat biasa yang produknya secara khas mengalam perubahan lebih lanjut. Kumparan kosubstrat gugus metabolit aktif berbeda dengan enzim yang mengkatalisis reaksi.
- Gugus prostetik terikat pada enzim selama jalannya reaksi, pada beberapa hal gugus prostetik terikat secara kovalen pada apoenzim yang pada kasus lain gugus prostetik terikat kuat pada sisi aktif dengan interaksi lemah. Seperti residu asam amino ionik pada sisi aktif , gugus prostetik akan kembali pada bentuk asalnya.
- Kosubstrat dan gugus prostetik merupakan bagian dari sisi aktif yang tdak terdapat pada rantai samping residu asam amino.
- Prokariot, protista, fungi, dan tumbuhan dapat mensintesis sendiri koenzim dari prekursor sedangkan mamalia membutuhkan sumber koenzim untuk bertahan hidup yang disuplai dari nutrisi (biasanya dalam jumlah kecil) yang disebut vitamin.
- Sumber utama vitamin dari tumbuhan dan organisme meskipun binatang karnivora dapat memenuhi vitamin dari daging. Sebagian besar vitamin akan diubah secara enzimatik menjadi koenzim koresponden
- Penyakit karena kekurangan nutrisi dapat terjadi saat vitamin sedikit atau tidak ada pada makanan seekor hewan namun dapat diatasi dan dicegah dengan mengkonsumsi vitamin yang tepat. Pemulihan dari penyakit tersebut telah digunakan untuk menguji potensi ekstrak selama isolasi vitamin.
- Sebagian besar vitamin akan dikonversi menjadi koenzim setelah bereaksi dengan ATP. Banyaknya molekul ATP yang ditransfer pada vitamin merupakan gugus yang mengikat koenzim pada sisi aktif enzim.
- Kata vitamin diciptakan oleh Casimir Funk pada tahun 1912 untuk mendeskripsikan “vital amin” dari sekam beras yang menyembuhkan penyakit beri-beri (penyakit kekurangan nutrisi yang berakibaat pada kemunduran syaraf). Beri-beri pertama kali ditemukan pada burung. Substansi anti beri-beri (tiamin) dikenal sebagai vitamin B1.
- Dua klasifikasi vitamin: vitamin larut air (seperti vitamin B) dan vitamin larut lemak (vitamin lemak). Vitamin larut air dibutuhkan tiap harinya dalam jumlah yang sedikit karena vitamin ini dieksresi dengan cepat pada urin dan penyimpanan selular dan koenzimnya tidak stabil. Vitamin larut lemak seperti vitamin A, D, E, K disimpan oleh hewan dan kelebihan asupan vitamin dapat berakibat toksik yang disebut hiperavitaminosis.
Baca Juga Artikel Yang Mungkin Berhubungan : Pengertian Enzim Laktase Pada Pencernaan
Fungsi Koenzim
Pada koenzim ini berfungsi sebagai pembawa sementara produk setengah reaksi. Mereka biasanya berpartisipasi dalam interaksi substrat-enzim dengan menyumbang atau menerima gugus kimia tertentu. Sebuha koenzim selalu mendapatkan kembali bentuk aslinya meskipun mungkin telah diubah selama reaksi. Banyak vitamin yang merupakan precursor dari koenzim. contohnya saja seperti: vitamin B yang berfungsi sebagai koenzim penting bagi enzim untuk membentuk lemak, karbohidrat dan protein.
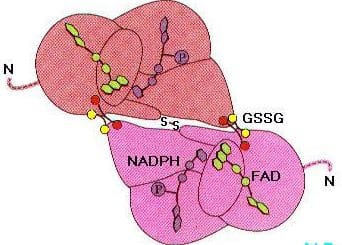
Koenzim merupakan salah satu dari sejumlah senyawa organik bebas yang menyebar yang memiliki fungsi sebagai kofaktor dengan enzim dalam meningkatkan berbagai reaksi metabolisme. Koenzim berpartisipasi dalam katalisis yang dimediasi enzim stoikiometri, dimodifikasi selama reaksi dan mungkin memerlukan reaksi yang dikatalisasi enzim lain untuk mengembalikan mereka ke keadaan aslinya.
Contohnya termasuk nikotinamida adenin dinukleotida (NAD) yang menerima hydrogen dan memberikan itu dalam reaksi lain dan ATP, yang memberikan kelompok-kelompok fosfat sementara mentransfer energi kimia dan mengambil kembali fosfat dalam reaksi lain. Sebagian besar vitamin B (lihat vitamin B kompleks) merupakan koenzim dan sangat penting dalam memfasilitasi transfer atom atau kelompok atom antara molekul dama pembentukan karbohidrat, lemak dan protein.
Baca Juga Artikel Yang Mungkin Berhubungan : Perbedaan Koenzim Dan Kofaktor Dalam Biologi
Enzim Kation Anorgnik
Enzim Yang Membutuhkan Kation Anorgnik adalah sebagai berikut :
- Enzim membutuhkan kation metal untuk mencapai aktivitas katalitik lengkap.
- Enzim dibedakan menjadi 2 tipe yaitu enzim yang diaktivasi oleh logam dan metaloenzim. Enzim yang diaktivasi oleh logam membutuhkan penambahan iom logam atau distimulasi oleh penambahan ion logam. Bebrapa enzim membutuhkan kation monovalen seperti K+ atau divalen seperti Ca2+ atau Mg2+. Contoh:kinase membutuhkan ion Mg2+ untuk membentuk kompleks magnesium- ATP dan menggunakan gugus fosforil substrat. Magnesium diserang oleh gugus fosfat pada ATP melalui muatan negatifnya sehingga lebih rentan terhadap serangan nukleofilik.
- Metaloenzim terikat kuat pada ion metal di sisi aktifnya. Ion yang paling umum ditemukan pada mealoenzim adalah logam transisi sepertibesi dan zink dan juga Cu dan Co.
- Ion logam yang terikat kuat pada enzim biasanya memiliki peran penting pada reaksi katalisis. Ion dari beberapa metaloenzim dapat bertindak sebagai katalis elektrofilik yaitu dengan menarik elektron sehingga ikatan dapat terpolarisasi. Contoh: enzim karbonat anhidrase adalah elektrofilik atom zink yang terikat dengan rantai samping dari tiga residu histidin dan sebuah molekul air karena air terionisasi dengan mudah. Gugus karboksilat dasar dari enzim melepaskan sebuah proton dari ikatan molekul air menghasilkan ion hidroksida nukleofilik yang menyerang substrat. Enzim ini memiliki laju katalisis yang sangat tinggi karena kesederhanaan mekanismenya. Banyak metaloenzim zink lain yang mengaktivasi ikatan molekul air pada cara ini.
Baca Juga Artikel Yang Mungkin Berhubungan : Penjelasan Sumber Enzim Laktase Dalam Biologi
Perbedaan Koenzim Dan Kofaktor
Koenzim
Berdasarkan strukturnya, enzim terdiri atas komponen yang disebut apoenzim yang berupa protein dan gugus protetik berupa non protein.Gugus prostetik dibedakan menjadi koenzim dan kofaktor.
Gugus koenzim tersusun dari senyawa organik nonprotein yang tidak melekat erat pada bagian protein enzim. Fungsi koenzim adalah membantu proses katalisis oleh enzim maupun penyusunan struktural yang penting. Koenzim digunakan untuk memantapkan ikatan antara substrat pada enzim atau mentransfer elektron yang timbul selama proses katalisa. Contoh koenzim adalah NADH, NADPH dan adenosina trifosfat.
Gugus kimiawi yang dibawa mencakup :
- Ionhidrida(H –) yang dibawa olehNAD atau NADP+
- Gugus asetil yang dibawa oleh koenzim A
- Formil, metenil dibawa oleh asam folat
- Gugus metil yang dibawa oleh S-adenosilmetionina.
Ada beberapa koenzim lain seperti riboflavin, tiamina, dan asam folat adalah vitamin.
Koenzim merupakan senyawa organik yang diperlukan untuk aktifitas suatu enzim tertentu yang bersifat termostabil dan memiliki berat molekul rendah.Koenzim akan memperbesar kemampuan katalitik sebuah enzim sehingga menjadi jauh melebihi kemampuan yang ditawarkan hanya oleh gugus fungsional asam aminonya, yang menyusun massa enzim tersebut.
Koenzim yang berikatan secara erat dengan enzim lewat ikatan kovalen atau gaya nonkovalen kerap kali disebut sebagai gugus prostetik. Koenzim yang mampu berdifusi secara bebas umumnya berfungsi sebagai unsur pembawa (yang didaur ulang secara kontinu) hydrogen (FADH), hidrida (NADH dan NADPH), atau unit-unit kimia seperti gugus asil (koenzim A) atau gugus metil (folat), membawanya bolak-balik antara tempat pembentukannya dan pemakaiannya. Oleh karena itu, koenzim yang disebut sebagai substrat sekunder.
Jenis-jenis enzim yang membutuhkan koenzim adalah enzim yang mengatalisis reaksi oksidasireduksi, pemindahan gugus serta isomerisasi, dan reaksi yang membentuk ikatan kovalen (kelas IUB 1,2,5, dan 6).
Kofaktor
Kofaktor berfungsi sama dengan gugus prostetik, tetapi berikatan secara reversible Dapat berupa zat anorganik
- ion logam (Metal- activated enzymes)
Dapat berupa zat organik - flavin dan heme
Contoh enzim yg mengandung kofaktor;
karbonat anhidrase dg kofaktor Zn terikatsbg bgn dari tapak aktifnya ->katalitik
Pembagian Kofaktor;
- Aktivator
ion anorganik yang biasanya berikatan lemah dengan suatu enzim
Contoh; Cu,Fe,Mn,Zn.Ca,K dan Co - Ggs Prostetik -> ikatan kovalen
dapat berupa senyawa,organik ttt,vitamin / ionlogam
Contoh:
FAD -> Vit,B2/Riboflavin -> menerima atom hidrogen
Ion Logam: Sitokrom ->sebagai pembawa elektron pada Fe
Koenzim berupa gugus organik yang padaumumnya merupakan vitamin, seperti vitamin B1, B2, NAD+ (Nicotinamide Adenine Dinucleotide ).
Kofaktor berupa gugus anorganik yang biasanya berupa ion-ion logam, seperti Cu2+, Mg2+, dan Fe2+
Kofaktor adalah komponen enzim yangbersifat non-protein yang berfungsimengaktifkan enzim.
Sifatnya stabil terhadap perubahan suhuatau suatu reaksi.
Kofaktor dibedakan menjadi tiga tipe yaitu, aktivator, gugus prostetik dan ko-enzim
- Aktivator
Aktivator adalah ion – ion anorganik yangbiasanya berikatan lemah dengan suatuenzim. Contoh beberapa logam berperansebagai aktivator dalam sistem enzimadalah Cu, Fe, Mn, Zn, Ca, K dan Co. - Gugus Prostetik
Gugus prostetik berikatan erat denganenzim (protein) oleh ikatan kovalen.Gugus prostetik dapat berupa senyawaorganik tertentu, vitamin atau ion logam.Misal FAD yang mengandung riboflavin (Vitamin
B2) yang merupakan bagian FADyang menerima atom Hidrogen. - Koenzim
Enzim yang tidak mempunyai gugusprostetik, memerlukan senyawa organiklain untuk aktivitasnya juga disebutkoenzim. Koenzim tidak melekat erat padabagian protein enzim.
Baca Juga Artikel Yang Mungkin Berhubungan : Gangguan Proses Metabolisme – Pengertian, Karbohidrat, Asidosis, Fenilketorunia, Hipertiroid, Addison, Protein, Lemak
Perbedaan Enzim dan Koenzim
- Enzim
• Merupakan suatu biokatalisator
• Bersifat termolabil
• Bersifat spesifik dalam melaksanakan fungsinya
• Dirusak oleh logam berat
• Aktifitas enzim diukur dengan kecepatan reaksi enzimatik
• Letak enzim tertentu didalam sel
• Hanya mengkatalis satu macam reaksi
- Koenzim
• Senyawa organik yang diperlukan untuk aktifitas suatu enzim tertentu
• bersifat termostabil
• Berat molekul rendah
• Banyak koenzim yang merupakan derivat vitamin B
• Bisa di anggap sebagai substrat kedua.
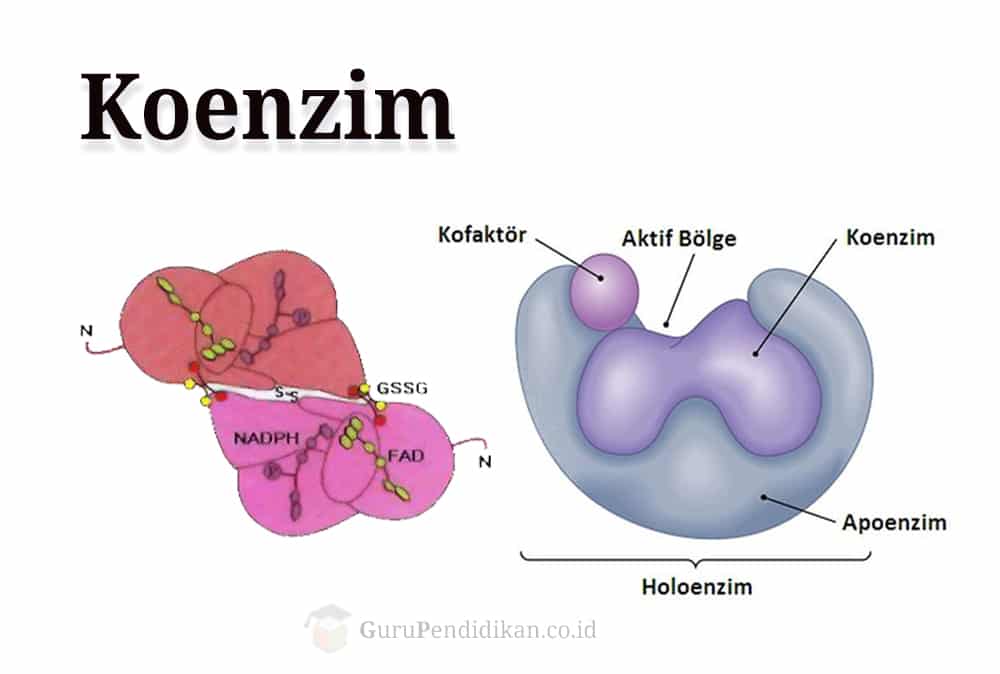
Komponen Penyusun
Struktur enzim yang sempurna dan aktif mengkatalisis bersama-sama dengan koenzim atau gugus logamnya disebut dengan holoenzim. Holoenzim merupakan keseluruhan molekul enzim yang meliputi apoenzim dan kofaktor. Penyusun utama suatu enzim adalah molekul protein yang disebut Apoenzim. Apoenzim adalah suatu polipeptida yang mempunyai struktur tersier atau kuartener dengan urutan dan komposisi asam amino tertentu dan rantai polipeptida tersebut distabillkan oleh ikatan sulfida, ikatan hidrogen, dan ikatan Van der Waals. Apoenzim bersifat labil (mudah berubah) yang dipengaruhi oleh suhu dan keasaman.
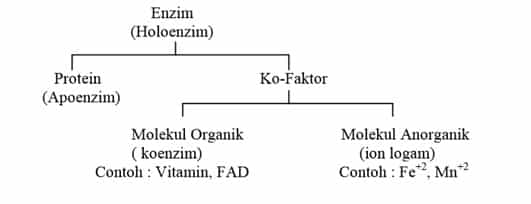
Enzim memerlukan komponen lain yaitu kofaktor agar berfungsi dengan baik. Kofaktor akan terikat pada gugus aktif pada molekul protein enzim, sehingga kerja enzim yang ditunjukkan oleh aktivitas meningkat (Lehninger, 1982). Secara ringkas struktur sebuah enzim dapat dilihat pada bagan di bawah ini :
Kofaktor pada beberapa enzim dapat terikat secara lemah atau terikat secara kuat (permanent). Jika kofaktor terikat kuat dengan protein enzim dinamakan bagian prostetik. Tidak semua enzim memiliki struktur yang lengkap terdiri dari apoenzim dan kofaktor. Contoh enzim ribonuklease pankreas hanya terdiri atas polipeptida dan tidak mengandung gugus kimiawi yang lain. Berdasarkan ikatannya, kofaktor dapat dibagi menjadi tiga kelompok, yaitu :
- Gugus prostetik
Tipe kofaktor yang biasanya terikat kuat pada enzim, berperan memberi kekuatan tambahan terhadap kerja enzim. Gugus prostetik dapat dikelompokkan menjadi dua yaitu gugus prostetik yang tersusun dari bahan organik dan gugus prostetik yang tersusun dari bahan anorganik.Contohnya adalah heme, yaitu molekul berbentuk cincin pipih yang mengandung besi. Heme merupakan gugus prostetik sejumlah enzim, antara lain katalase, peroksidase, dan sitokrom oksidase.
- Koenzim
Bagian dari gugus prostetik bukan protein. Kofaktor yang terdiri atas molekul organik nonprotein yang terikat renggang dengan enzim. Koenzim berfungsi untuk memindahkan gugus kimia, atom, atau elektron dari satu enzim ke enzim yang lain. Contohnya FAD (flavin adenina dinukleotida), tiamin pirofosfat, NAD, NADP+, dan asam tetrahidrofolat.
- Ion-ion anorganik
Kofaktor yang terikat dengan enzim atau substrat kompleks sehingga fungsi enzim lebih efektif. Contohnya, amilase dalam ludah akan bekerja lebih baik dengan adanya ion klorida dan kalsium. Beberapa kofaktor tidak berubah di akhir reaksi, tetapi kadang-kadang berubah dan terlibat dalam reaksi yang lain. Ion anorganik dapat berupa ion logam yang berasosiasi dengan apoenzim dan diperlukan untuk aktivitas enzim tertentu. Ion logam tersebut berikatan dengan apoenzim melalui ikatan koordinasi
Beberapa jenis logam sebagai bagian kofaktor dari beberapa enzim dapat dilihat pada Tabel 1 dan Tabel 2.
Contoh reaksi yang menggunakan bagian protein dan bukan protein :