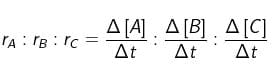Laju Reaksi : Pengertian, Faktor Yang Mempengaruhi, Dan Rumus Beserta Contoh Soalnya Lengkap
Konsep pembelajaran kimia merupakan konsep yang erat dengan kehidupan sehari hari. Kimia menggambarkan kehidupan sedemikian rupa sehingga terlihat lebih rinci dan beragam. Hal ini lah yang membuat para pengajar menerapkan konsep kimia ke dalam kehidupan sehari-hari dengan menghadirkannya dalam contoh-contoh sederhana. Selain itu, juga dilakukan pengenalan terhadap konsep-konsep yang sering digunakan dalam dunia luas, bahkan kebiasaan yang sederhana yang sering kita lakukan tanpa kita ketahui itu merupakan konsep kimia.
Salah satu contohnya yaitu pada konsep laju reaksi dalam kimia. Dalam kimia dijelaskan bahwasanya laju reaksi adalah adalah besarnya perubahan jumlah pereaksi dan hasil reaksi per satuan waktu. Perubahan ini dapat dikatakan perubahan konsentrasi molar (molaritas) sehingga laju reaksi dapat dikatakan perubahan konsentrasi akhir (hasil reaksi) terhadap konsentrasi awal (pereaksi) per satuan waktu.
Banyak sekali konsep laju reaksi yang kita temukan dalam kehidupan sehari-hari. Oleh karena itu, dalam makalah ini akan dijelaskan secara rinci manfaat laju reaksi dalam kehidupan sehari-hari.
Pengertian Laju Reaksi
Laju reaksi merupakan laju penurunan reaktan (pereaksi) atau laju bertambahnya produk (hasil reaksi). Laju reaksi ini juga menggambarkan cepat lambatnya suatu reaksi kimia, sedangkan reaksi kimia merupakan proses mengubah suatu zat (pereaksi) menjadi zat baru yang disebut dengan produk.
Beberapa reaksi kimia ada yang berlangsung cepat. Natrium yang dimasukkan ke dalam air akan menunjukkan reaksi hebat dan sangat cepat, begitu pula dengan petasan dan kembang api yang disulut. Bensin akan terbakar lebih cepat daripada minyak tanah. Namun, ada pula reaksi yang berjalan lambat. Proses pengaratan besi, misalnya, membutuhkan waktu sangat lama sehingga laju reaksinya lambat.
Cepat lambatnya proses reaksi kimia yang berlangsung dinyatakan dengan laju reaksi. Dalam mempelajari laju reaksi digunakan besaran konsentrasi tiap satuan waktu yang dinyatakan dengan molaritas. Apakah yang dimaksud molaritas? Simak uraian berikut.
Molaritas sebagai Satuan Konsentrasi dalam Laju Reaksi
Molaritas menyatakan jumlah mol zat dalam 1 L larutan, sehingga molaritas yang dinotasikan dengan M, dan dirumuskan sebagai berikut.
M = n/V
Keterangan :
n = jumlah mol dalam satuan mol atau mmol
V = volume dalam satuan L atau mL
Manfaat Laju Reaksi
-
dalam Kehidupan Sehari-Hari
Dengan mempelajari laju reaksi kita dapat mengetahui bahwa reaksi itu dapat berlangsung dipengaruhi oleh beberapa faktor, misalnya saja luas permukaan. Jika kita mengetahui bahwa luas permukaan itu mempengaruhi laju reaksi, pasti kita akan memperkecil luas permukaan suatu zat sebelum mengolahnya.
- Beberapa contoh penerapan Laju Reaksi dalam kehidupan sehari hari :
- Ibu di rumah atau pedagang bubur kacang mengiris terlebih dahulu gula merah yang akan di masukan ke dalam bubur kacang.
- Penduduk pedesaan membelah kayu gelondongan menjadi beberapa bagian sebelum dimasukkan ke dalam tungku perapian.
- Penjual gado-gado, lontong, dan pecel terlebih dulu menggerus kacang goreng sebelum dicampurkan dengan bahan lain.
- Dalam pembuatan kertas, bahan baku pembuat kertas digerus terlebih dahulu untuk membuat bubur kertas. Agar memperluas pemukaan bidang sentuh sehingga campuran menjadi homogen danreaksi berlangsung sempurna.
- Bahan baku yang sering di tambang, tersedia dalam bentuk butir-butiran kasar. Untuk mempercepat pengolahan selanjutnya, butiran-butiran tersebut dihancurkan sampai halus.
- Dalam pembuatan roti kita bisa menambahkan ragi yang berfungsi sebagai katalis untuk mempercepat laju reaksinya.
Faktor Laju Reaksi
Faktor-faktor yang mempengaruhinya antara lain:
-
1. Konsentrasi Reaktan
Semakin tinggi konsentrasi reaktan, semakin banyak jumlah partikel reaktan yang bertumbukan, sehingga semakin tinggi frekuensi terjadinya tumbukan dan lajunya meningkat. Sebagai contoh, dalam reaksi korosi besi di udara, laju reaksi korosi besi lebih tinggi pada udara yang kelembabannya lebih tinggi (konsentrasi reaktan H2O tinggi)
-
2. Suhu
Suhu juga turut berperan dalam mempengaruhi laju reaksi. Apabila suhu pada suatu reaksi yang berlangusng dinaikkan, maka menyebabkan partikel semakin aktif bergerak, sehingga tumbukan yang terjadi semakin sering, menyebabkan laju reaksi semakin besar. Sebaliknya, apabila suhu diturunkan, maka partikel semakin tak aktif, sehingga laju reaksi semakin kecil.
-
3. Tekanan
Banyak reaksi yang melibatkan pereaksi dalam wujud gas. Kelajuan dari pereaksi seperti itu juga dipengaruhi tekanan. Penambahan tekanan dengan memperkecil volume akan memperbesar konsentrasi, dengan demikian dapat memperbesar laju reaksi.
-
4. Keberadaan Katalis
Katalis adalah suatu zat yang mempercepat laju reaksi kimia pada suhu tertentu, tanpa mengalami perubahan atau terpakai oleh reaksi itu sendiri. Suatu katalis berperan dalam reaksi tapi bukan sebagai pereaksi ataupun produk. Katalis memungkinkan reaksi berlangsung lebih cepat atau memungkinkan reaksi pada suhu lebih rendah akibat perubahan yang dipicunya terhadap pereaksi. Katalis menyediakan suatu jalur pilihan dengan energi aktivasi yang lebih rendah. Katalis mengurangi energi yang dibutuhkan untuk berlangsungnya reaksi.
-
5. Luas Permukaan Sentuh
Luas permukaan sentuh memiliki peranan yang sangat penting dalam laju reaksi, sebab semakin besar luas permukaan bidang sentuh antar partikel, maka tumbukan yang terjadi semakin banyak, sehingga menyebabkan laju reaksi semakin cepat.
Begitu juga, apabila semakin kecil luas permukaan bidang sentuh, maka semakin kecil tumbukan yang terjadi antar partikel, sehingga laju reaksi pun semakin kecil. Karakteristik kepingan yang direaksikan juga turut berpengaruh, yaitu semakin halus kepingan itu, maka semakin cepat waktu yang dibutuhkan untuk bereaksi; sedangkan semakin kasar kepingan itu, maka semakin lama waktu yang dibutuhkan untuk bereaksi.
Rumus Laju Reaksi
Laju reaksi kimia bukan hanya sebuah teori, namun dapat dirumuskan secara matematis untuk memudahkan pembelajaran. Pada reaksi kimia: A → B, maka laju berubahnya zat A menjadi zat B ditentukan dari jumlah zat A yang bereaksi atau jumlah zat B yang terbentuk per satuan waktu. Pada saat pereaksi (A) berkurang, hasil reaksi (B) akan bertambah. Perhatikan diagram perubahan konsentrasi pereaksi dan hasil reaksi pada Gambar 3.
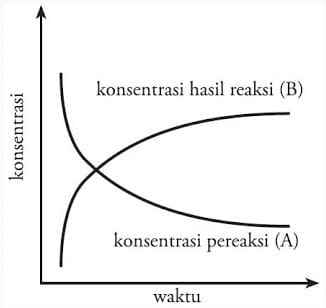
Berdasarkan gambar tersebut, maka rumusan laju reaksi dapat kita definisikan sebagai:
a. berkurangnya jumlah pereaksi (konsentrasi pereaksi) per satuan waktu, atau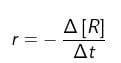 , dengan r = laju reaksi, – d[R] = berkurangnya reaktan (pereaksi), dan dt = perubahan waktu. Untuk reaksi : A → B, laju berkurangnya zat A adalah :
, dengan r = laju reaksi, – d[R] = berkurangnya reaktan (pereaksi), dan dt = perubahan waktu. Untuk reaksi : A → B, laju berkurangnya zat A adalah : ![]()
b. bertambahnya jumlah produk (konsentrasi produk) per satuan waktu, atau 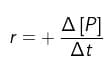 , dengan +Δ[P] = bertambahnya konsentrasi produk (hasil reaksi). Untuk reaksi : A → B, laju bertambahnya zat B adalah :
, dengan +Δ[P] = bertambahnya konsentrasi produk (hasil reaksi). Untuk reaksi : A → B, laju bertambahnya zat B adalah : 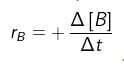
Bagaimana untuk reaksi yang lebih kompleks, semisal : pA + qB → rC.
Untuk reaksi demikian, maka :
Dalam perbandingan tersebut, tanda + atau – tidak perlu dituliskan karena hanya menunjukkan sifat perubahan konsentrasi. Oleh karena harga dt masing-masing sama, maka perbandingan laju reaksi sesuai dengan perbandingan konsentrasi. Di sisi lain, konsentrasi berbanding lurus dengan mol serta berbanding lurus pula dengan koefisien reaksi, sehingga perbandingan laju reaksi sesuai dengan perbandingan koefisien reaksi. Perbandingan tersebut dapat dituliskan sebagai berikut.
rA : rB : rC = p : q : r
-
JURNAL PERCOBAAN LAJU REAKSI DAN PEMBAHASAN
ALAT DAN BAHAN
> ALAT
| 1. | tabung reaksi | (6 buah) |
| 2. | rak tabung reaksi | (1 buah) |
| 3. | stopwatch | (1 buah) |
| 4. | kertas hvs | (1 lembar) |
| 5. | gelas beaker 100ml | (2 buah) |
| 6. | water bath | (1 buah) |
| 7. | thermometer | (1 buah) |
| 8. | pipet tetes | (2 buah) |
| 9. | neracaohaus | (1 buah) |
| 10. | gelas ukur | (1 buah) |
| 11. | alu dan mortar | (1 buah) |
| 12. | spatula | (1 buah) |
| 13. | cawan petri | (1 buah) |
| 14. | penjepit kayu | (1 buah) |
| 15. | spidol | (1 buah) |
| BAHAN | ||
| 1. | pita magnesium | (4 pcs Masing-masing 0,5 cm) |
| 2. | HCl 0,1M | (15 ml) |
| 3. | HCl 0,5M | (1 ml) |
| 4. | HCl 1M | (1ml) |
| 5. | HCl 2M | (1ml) |
| 6. | HCl 3M | (1ml) |
| 7. | Na2S2O3 | (15 ml) |
| 8. | NaCl 0,1M | (4 tetes) |
| 9. | FeCl3 0,1M | (4 tetes) |
| 10. | H2O2 | (15 ml) |
| 11. | Marmer Serbuk | (1 gram) |
| 12. | Marmer Bongkahan | (1 gram) |
- METODE KERJA
Percobaan 1
|
Percobaan 2
|
| 4 | masukan thermometer
kedalam gelas beaker untu mengukur suhu awal Na2S2O3 |
suhu 29oc |
| 5 | dituangkan HCl 0,1M
kedalam gelas ukur sebanyak 15 ml |
tidak terjadi reaksi |
| 6 | Dituangkan HCl kedalam gelas beaker berisi
Na2S2O3 0,1M yang berada di atas kertas yang telah ditandai |
Terjadi perubahan warna yaitu berwarna putih susu dan larutan berbau |
| 7 | panaskan Na2S2O3 dan HCl masing-masing 15 ml
didalam water bath sampai suhu (60,50,40)oc |
Larutan menjadi panas karena suhu meningkat setelah dipanaskan |
| 8 | dituangkan HCl dan
Na2S2O3 secara bersamaan kedalam gelas beaker diatas kertas yang telah ditandai |
Larutan menjadi berwarna putih susu sampai tanda X tidak tampak. Pada suhu:
60oC= 52s 50oC = 107s 40oC = 122s |
Percobaan 3
|
Percobaan 4
|
| 2 | Dituangkan H2O2 kedalam 3 tabung reaksi masing-masing 5 ml | Tidak terjadi reaksi |
| 3 | – Tabung 1 sebagai control
– Tabung 2 ditambahkan FeCl3 sebanyak 4 tetes – Tabung 3 ditambahkan NaCl 4 tetes |
– Tabung 1 tidak terjadi reaksi
– Tabung 2 awalnya terbentuk 2 lapisan coklat tua dan bening, keluar asap, mendidih, terbentuk uap di dinding tabung, tabung panas, warna menjadi nyatu yaitu berwarna coklat muda. – Tabung 3 terbentuk gelembung dalam jumlah banyak. |
- ANALISIS DATA
A. Faktor konsentrasi terhadap laju reaksi
Reaksi : Mg(s) + 2HCl(aq) ————– ► MgCl2(aq) + H2(g) |
B. Faktor suhu pada terhadap reaksi
Na2S2O3(aq) + HCl(aq) ————— ► SO2(g) + S(s) + 2NaCl(aq) + H2O |
C. Pengaruh luas permukaan terhadap laju reaksi
CaCO3(s) + 2HCl(aq) ————– ► CaCl2(s) + H2O(aq) + CO2(g) |
D. Pengaruh katalis terhadap laju reaksi
2 H2O2(aq) _ NaCl – 2H2O(l) + 02(g) |
|||||||||||||||
- PEMBAHASAN
Pada praktukum kali ini telah dilakukan percobaan yaitu mengenai laju reaksi. Terdapat empat faktor yang mempengaruhi laju reaksi diantaranya adalah konsentrasi, suhu, luas permukaan, dan katalis.
Pada percobaan pertama dilakukan pengamatan pengaruh konsentrasi terhadap laju reaksi yaitu dilakukan dengan cara mereaksikan pita magnesium (Mg) dengan HCl yang konsentrasinya berbeda-beda. pada tabung 1 terdapat hcl 0,5M, pada tabung 2 terdapat HCl 1M, pada tabung 3 terdapat HCl 2M, dan pada tabung 4 terdapat HCl 3M. pada tabung 1 laju reaksi bejalan sangat lambat yaitu 234s, pada tabung kedua laju reaksi berjalan agak cepat yaitu 104s, pada tabung 3 laju reaksi berjalan cepat yaitu 28s, dan pada tabung 4 laju reaksi berjalan cepat yaitu 11s.
sudah terbukti bahwa semakin ditingkatkan konsentrasi hcl, maka laju reaksi semakin berjalan dengan cepat. hal ini membuktikan bahwa konsentrasi mempengaruhi laju reaksi. jika konsentrasi suatu zat semakin besar maka laju reaksinya semakin cepat dan begitupun sebaliknya semakin kecil konsentrasi suatu zat maka laju reaksi akan berjalan lambat. suatu larutan dengan konsentrasi tinggi akan lebih pekat dan mengandung partikel yang lebih rapat sehingga akan lebih sering bertumbukan. Berdasarkan percobaan yang telah dilakukan, dapat dilihat bahwa hasil pengamatan kami sesuai dengan teori dari laju reaksi yaitu semakin besar konsentrasi suatu larutan makan semakin cepat laju reaksi yang terjadi.
Pada percobaan kedua dilakukan percobaan pengaruh suhu terhadap laju reaksi. pencampuran hcl dengan Na2S2O3 yang berbeda-beda yaitu pada suhu ruangan 29oC dan suhu setelah dipanaskan yaitu pada suhu (40, 50, 60) oC. pada saat Na2S2O3 pada suhu 29 oC diperlukan waktu yag cukup lama sampai warna larutan berwarna putih susu yaitu 170s. ketika suhu dinaikan menjadi 40 oC waktu yag diperlukan lebih singkat yaitu 122s. kemudian suhu dinaikan lagi menjadi 50 oC waktu yang diperlukanpun lebih singkat lagi yaitu 107s. dan terakhir kita menaikan suhu menjadi 60 oC waktu yag diperlukan sangat singkat yaitu 52s.
hal ini terjadi karena suhu ikut berperan dalam mempengaruhi laju reaksi apabila suhu yag berlangsung pada suatu reaksi yang berlangsung dinaikan, maka menyebabkan partikel semakin aktif bergerak, sehingga tumbukan yang terjadi lebih sering terjadi, hal itu menyebabka laju reaksi semakin cepat. sebaliknya apabila suhu diturunkan, maka partikel semakin tidak aktif, sehingga laju reaksi semakin lambat. hal ini sesuai dengan teori laju reaksi yaitu semakin tinggi suhu, maka semakin cepat laju reaksi yang terjadi.
Pada percobaan ketiga dilakukan percobaan pengaruh luas permukaan terhadap laju reaksi. berdasarkan percobaan, batu marmer yang telah dihaluskan sebanyak 1 gram yang direaksikan dengan 5ml HCl 2M bereaksi lebih cepat dibandingkan dengan bongkahan marmer sebanyak 1 gram yang direaksikan dengan 5ml HCl 2M. berdasarkan teori, bubuk zat padat biasanya menghasilkan reaksi yag lebih cepat dibandingkan dengan sebuah bongkahan zat padat dengan massa yang sama, karena bubuk zat padat memiliki luas permukaan yag lebih besar.
suatu zat akan bereaksi hanya jika zat tersebut bercampur dan terjadi tumbukan. tumbuka tersebut terjadi antara tumbukan luas permukaan bidang sentuh dari masing-masing molekul. semakin kecil ukuran partikel zat maka semakin luas permukaan suatu zat. jadi, semakin kecil ukuran partikel zat, maka reaksipun akan berlangsung cepat. hal ini sesuai dengan konsep laju rreaksi yaitu semakin besar luas permukaan, maka laju reaksi semakin cepat.
Pada percobaan terakhir yaitu pengamatan katalis dalam laju reaksi. kalis adalah suatu zat yang mempercepat laju reaksi pada suhu tertentu, tanpa mengalami perubahan dalam reaksi itu sendiri. suatu katalis berperan dalam reaksi tapi bukan sebagai pereaksi ataupun produk. dalam percobaan kami menggunakan dua katalis yag berbeda, yaitu nac dan FeCl3. digunakan tiga tabung reaksi, tabung pertama berisi 5ml H2O2 dijadikan sebagai kontrol yang tidak diperlakukan apa-apa. pada tabung kedua yaitu 5ml H2O2 dan ditambahkan 4 tetes naclkemudian terbentuk gelembung dalam jumlah banyak dan tidak mengalami perubahan warna.
pada tabung ketiga yang berisi 5ml H2O2 yang kemusian ditambhakan 4 tetes FeCl3 reaksi terjadi secara perlahan-lahan, pada awalnya terbentuk dua lapisan yaitu berwarna coklat tua dan bening kemudian keluar asap da menguap, larutan mendidih dan permukaan tabung reaksi terasa panas, warna larutanpun mulai tercampur dan terbentuk satu warna yaitu coklat muda. dari hasil pengamatan, dapat dilihat bahwa katalis yang cocok denga H2O2 adalah FeCl3. hal ini dapat terjadi karena sifat katalis seperti enzim, yaitu hanya bekerja pada senyawa tertentu. hasil pengamatan kami sesuai dengan konsep laju reaksi, yaitu katalis dapat mempengaruhi laju reaksi.
Persamaan Laju Reaksi
Secara umum, laju reaksi dapat dinyatakan dengan rumus :
Keterangan :
v = laju reaksi
k = konstanta laju reaksi ( nilainya tergantung pada jenis reaktan, suhu dan katalis )
x = orde atau tingkat reaksi terhadap reaktan A
y = orde atau tingkat reaksi terhadap reaktan B
x + y = orde atau tingkat reaksi total / keseluruhan
Harga k akan berubah jika suhu berubah. Kenaikan suhu dan penggunaan katalis umumnya akan memperbesar harga k.
Orde Reaksi
“ Orde reaksi menyatakan besarnya pengaruh konsentrasi reaktan terhadap laju reaksi. ”
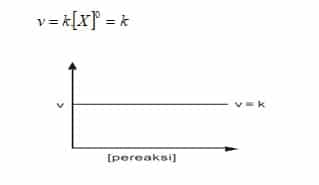
- Orde reaksi nol.
Reaksi dikatakan ber’orde nol terhadap salah satu reaktan, jika perubahan konsentrasi reaktan tersebut tidak mempengaruhi laju reaksi. Artinya, asalkan terdapat dalam jumlah tertentu; perubahan konsentrasi reaktan itu tidak mempengaruhi laju reaksi.
Besarnya laju reaksi hanya dipengaruhi oleh besarnya konstanta laju reaksi ( k ).
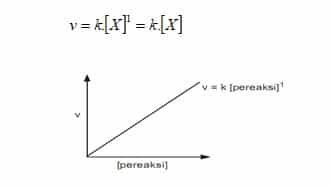
- Orde reaksi satu.
Suatu reaksi dikatakan ber’orde satu terhadap salah satu reaktan, jika laju reaksi berbanding lurus dengan konsentrasi reaktan itu.
Jika konsentrasi reaktan itu dilipat-tigakan maka laju reaksinya akan menjadi 31 atau 3 kali lebih besar.
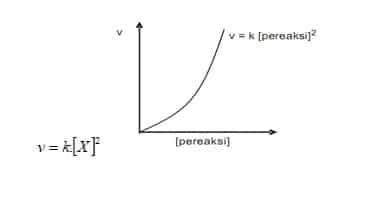
- Orde reaksi dua.
Suatu reaksi dikatakan ber’orde dua terhadap salah satu reaktan, jika laju reaksi merupakan pangkat dua dari konsentrasi reaktan itu.
Jika konsentrasi reaktan itu dilipat-tigakan, maka laju reaksi akan menjadi 32 atau 9 kali lebih besar.
Teori Tumbukan
- Suatu zat dapat bereaksi dengan zat lain jika partikel-partikelnya saling bertumbukan. Tumbukan yang terjadi akan menghasilkan energi untuk memulai terjadinya reaksi.
- Terjadinya tumbukan tersebut disebabkan karena partikel-partikel zat selalu bergerak dengan arah yang tidak teratur.
- Tumbukan antar partikel yang bereaksi tidak selalu menghasilkan reaksi. Hanya tumbukan yang menghasilkan energi yang cukup serta arah tumbukan yang tepat, yang dapat menghasilkan reaksi. Tumbukan seperti ini disebut tumbukan yang efektif.
Jadi, laju reaksi tergantung pada 3 hal :
- Frekuensi tumbukan
- Energi partikel reaktan
- Arah tumbukan
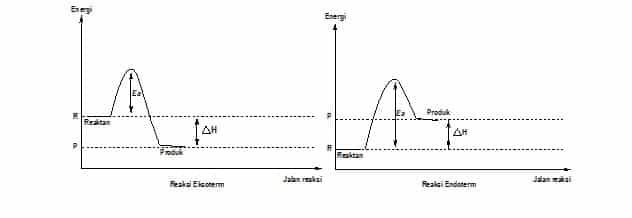
- Energi minimum yang harus dimiliki oleh partikel reaktan, sehingga menghasilkan tumbukan yang efektif disebut energi pengaktifan atau energi aktivasi ( Ea ).
- Semua reaksi, baik eksoterm maupun endoterm memerlukan Ea. Reaksi yang dapat berlangsung pada suhu rendah berarti memiliki Ea yang rendah. Sebaliknya, reaksi yang dapat berlangsung pada suhu yang tinggi, berarti memiliki Ea yang tinggi.
- Ea ditafsirkan sebagai energi penghalang ( barrier ) antara reaktan dengan produk. Reaktan harus didorong agar dapat melewati energi penghalang tersebut sehingga dapat berubah menjadi produk.
Contoh Soal Laju Reaksi
Pada reaksi pembentukan gas SO3 menurut reaksi: 2SO2(g) + O2(g) → 2SO3(g), sehingga diperoleh data sebagai berikut.
Tentukanlah:
a. Laju bertambahnya SO3
b. Laju berkurangnya SO2
c. Laju berkurangnya O2
Penyelesaian :
Diketahui :
Persamaan reaksi : 2SO2(g) + O2(g) → 2SO3(g)
Data konsentrasi (pada tabel).
Ditanyakan :
a. r SO3.
b. r SO2.
c. r O2.
Jawaban :
a. Δ[SO3] = [SO3]3 – [SO3]2 = 0,50 – 0,25 = 0,25 M
Δt = t3 – t2 = 40 – 20 = 20 s
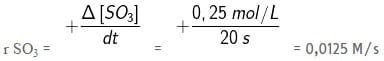
Jadi, laju bertambahnya SO3 sebesar 1,25 x 10–2 M/s.
b. Karena koefisien SO2 = koefisien SO3, maka:
r SO2 = – r SO3 = – 0,0125 M/s
Jadi, laju berkurangnya SO2 sebesar –1,25 x 10–2 M/s
c. r O2 = – ½ x r SO3 = – ½ x 0,0125 = – 0,00625 M/s
Jadi, laju berkurangnya O2 sebesar – 6,25 x 10–3 M/s
Itulah ulasan tentang Laju Reaksi : Pengertian, Faktor Yang Mempengaruhi, Dan Rumus Beserta Contoh Soalnya Lengkap Semoga apa yang diulas diatas bermanfaat bagi pembaca. Sekian dan terimakasih.
Baca juga refrensi artikel terkait lainnya disini :
- Larutan Elektrolit : Pengertian, Ciri, Dan Jenis Beserta Contohnya Secara Lengkap
- Larutan Buffer : Pengertian, Fungsi, Dan Jenis Beserta Contohnya Secara Lengkap
- Larutan Garam : Pengertian, Ciri, Dan Sifat Beserta Contohnya Secara Lengkap
- Larutan Basa : Pengertian, Ciri, Dan Sifat Beserta Contohnya Secara Lengkap
- Larutan Asam : Pengertian, Ciri, Dan Sifat Beserta Contohnya Secara Lengkap
- Pengertian, Ciri, Dan Sifat Asam, Basa, Dan Garam Beserta Contohnya Lengkap.
- video bokeh