Pengertian Helicobacter Pylori, Ciri, Diagnosis dan Pengobatan adalah bakteri yang menyebabkan peradangan lapisan lambung yang kronis (gastritis) pada manusia. Bakteri ini juga adalah penyebab yang paling umum dari borok-borok (ulcers) diseluruh dunia
Baca Juga Artikel Yang Mungkin Berhubungan : Penjelasan Ciri-Ciri Bacillus Anthracis Dalam Biologi
Pengertian Helicobacter Pylori
Helicobacter adalah nama genus kuman yang berbentuk spiral atau batang bengkok dan berflagela yang mengalami adaptasi untuk dapat hidup dalam mukus (lendir) lambung yang menutupi selaput lendir (mukosa) lambung yang bersuasana asam kuat. Kuman ini dapat bertahan hidup dalam suasana asam kuat dengan cara memproduksi enzim urease. Enzim urease akan mengubah urea yang ada dalam cairan lambung menjadi amoniak. Tubuh kuman Helicobacter selalu diliputi oleh awan amoniak ini, dan karenanya dapat bertahan terhadap asam lambung.
Kuman ini bersifat pleomorfik artinya dapat dijumpai dalam beberapa bentuk. Dalam keadaan normal kuman ini berbentuk spiral atau batang bengkok, tetapi dalam keadaan tertentu yang kurang baik akan merubah dirinya menjadi bentuk kokoid yang merupakan bentuk pertahanan yang resisten. Kuman ini termasuk kuman mikroaerofilik artinya hanya tumbuh dalam suasana dimana didapatkan oksigen dalam kadar rendah. Kuman ini mati pada suasana dengan kadar oksigen normal, dan mati dalam keadaan anaerobik sempurna.
Helicobacter pylori (H. pylori) adalah suatu bakteri yang menyebabkan peradangan lapisan lambung yang kronis (gastritis) pada manusia. Bakteri ini juga adalah penyebab yang paling umum dari borok-borok (ulcers) diseluruh dunia. Infeksi H. pylori kemungkinan besar didapat dengan memakan makanan dan air yang tercemar (terkontaminasi) dan melalui kontak orang ke orang. Di Amerika, 30% dari populasi orang dewasa terinfeksi. 50% dari orang-orang yang terinfeksi adalah terinfeksi pada umur 60 tahun. Infeksi lebih umum pada kondisi-kondisi hidup yang penuh sesak dengan sanitasi yang jelek. Pada negara-negara dengan sanitasi yang jelek, 90% dari populasi dewasa dapat terinfeksi. Individu-individu yang terinfeksi biasanya membawa infeksi terus menerus (tak terbatas) hingga mereka dirawat dengan obat-obat untuk membasmi bakteri. Satu dari setiap tujuh pasien dengan infeksi H. pylori akan mengembangkan borok-borok duodenum (usus dua belas jari) atau lambung. H. pylori juga berhubungan dengan kanker perut dan suatu tipe yang jarang dari tumor lymphocytic dari perut yang disebut MALT lymphoma. Mendiagnosis Infeksi Helicobacter Pylori
Infeksi Helicobacter pylori (Hp) pada saluran cema bagian atas mempunyai variasi klinis yang luas, mulai dari kelompok asimtomatik sampai tukak peptik, bahkan dihubungkan dengan keganasan di lambung seperti adenokarsinoma tipe intestinal atau mucosal associated lymphoid tissue (MAIJI) Limfoma
Kuman Helicobacter pylori bersifat mikroaerofilik dan hidup di lingkungan yang unik, dibawah mukus dinding lambung yang bersuasana asam. Kuman ini mempunyai enzim urease yang dapat memecah ureum menjadi amonia yang bersifat basa, sehingga tercipta lingkungan mikro yang memungkinkan kuman ini bertahan hidup. Karena itu prosedur diagnostik cukup sulit karena harus melakukan tindakan yang invasif yaitu dengan melakukan gastroskopi untuk mendapatkan spesimen yang diperlukan untuk pemeriksaan langsung, histopatologi ataupun kultur mikrobiologi. Selain itu terdapat pemeriksaan non invasif seperti tes serologi dan urea breath test (UBT).
Sebagian besar individu yang terkena infeksi H. pylori tidak mengalami keluhan walaupun pada pemeriksaan biopsi mukosa lambung pada kasus-kasus asimptomatik sebagian besar didapatkan gambaran gastritis kronik aktif.
Cara penegakkan diagnosa yang banyak dipakai dengan hasil yang baik adalah dengan diagnosa histologis.Cara lain adalah tes napas urea (urea breath test) dan pemeriksaan serologik. Kedua cara ini tidak memerlukan endoskopi.Belakangan ini ditemukan cara diagnosa infeksi H. pylori dengan cara deteksi antigen kuman H. pylori pada tinja penderita dengan metoda Elisa
Baca Juga Artikel Yang Mungkin Berhubungan : Penjelasan Ciri-Ciri Clostridium Tetani Dalam Biologi
Epidemiologi Helicobacter Pylori
Prevalensi infeksi Helicobacter Pylori di negara berkembang lebih tinggi dibandingkan negara maju. Prevalensi pada populasi negara maju sekitar 30-40%, sedangkan di negara berkembang mencapai 80-90%. Dari jumlah tersebut hanya sekitar 10-20% yang akan menjadi penyakit gastroduodenal.
Studi seroepidemiologi di Indonesia menunjukkan prevalensi 36-46,1% dengan usia termuda 5 bulan. Pada kelompok usia muda dibawah 5 tahun 5,3-15,4% telah terinfeksi, dan diduga infeksi pada usia dini berperan sebagai faktor resiko timbulnya degenerasi maligna pada usia yang lebih lanjut, karena kenyataannya prevalensi kanker lambung di indonesia relatif rendah, demikian pula prevalensi tukak peptik. Agaknya selain faktor bakteri, faktor pejamu dan faktor lingkungan yang berbeda akan menentukan terjadinya kelainan patologis akibat infeksi.
Secara umum telah diketahui bahwa infeksi HP merupakan masalah global, tetapi mekanisme transmisi apakah oral-oral atau fekal oral belum diketahui dengan pasti. Studi di Indonesia menunjukkan hubungan antara tingkat sanitasi lingkungan dengan prevalensi infeksi HP, sedangkan data diluar negeri menunjukkan hubungan antara infeksi dengan penyediaan atau sumber air minum.
Data penelitian klinis di Indonesia menunjukkan bahwa prevalensi tukak peptik pada pasien dispepsia yang di endoskopi berkisar antara 5,78% di Jakarta sampai 16,91 % di medan. Data penelitian prevalensi infeksi HP pada pasien tukak peptik dapat dilihat pada tabel 1.
Tabel 1. Prevalensi HP pada pasien tukak peptik di Indonesia
|
Peneliti |
Daerah |
Tukak |
Metoda Diagnosis |
Prevalensi (%) |
| Manan CH | Jakarta | Duodeni | CLO | 100 |
| Jayapranata | Surabaya | Duodeni | CLO | 93,9 |
| Jayapranata | Surabaya | Gaster | CLO | 85,7 |
Pada kelompok pasien dispepsia non ulkus. Prevalensi infeksi HP yang dilaporkan berkisar antara 20-40%, dengan metoda diagnostik yang berbeda yaitu seologi, kultur dan histopatologi. Angka tersebut memberi gambaran bahwa pola infeksi di Indonesia tidak terjadi pada usia dini tetapi pada usia yang lebih lanjut, tidak sama dengan pola negara berkembang lain seperti di Afrika. Agaknya yang berperan adalah faktor lingkungan dan juga faktor perbedaan ras.
Tingginya prevalensi infeksi dalam masyarakat tidak sesuai dengan prevalensi penyakit SCBA seperti tukak peptik ataupun karsinoma lambung. Diperkirakan hanya sekitar 10-20% saja yang menimbulkan penyakit gastroduodenal.
Strain Helicobacter Pylori yang Patogen
Infeksi Helicobacter pylori (Hp) pada saluran cema bagian atas mempunyai variasi klinis yang luas, mulai dari kelompok asimtomatik sampai tukak peptik, bahkan dihubungkan dengan keganasan di lambung seperti adenokarsinoma tipe intestinal atau mucosal associated lymphoid tissue (MAIJI) Limfoma.
Data epidemiologis dari berbagai bagian duniamenunjukkan adanya perbedaan geografis dan juga korelasi yang tidak sesuai antara prevalensi infeksi dengan prevalensi spektrum klinis seperti tukak peptik ataupun kanker lambung. Di Indonesia prevalensi Hp berdasarkan studi seroepidemilogi termasuk cukup tinggi, tetapi sebaliknya prevalensi berbagai keiainan klinis seperti tukak peptik maupun kanker lambung sangat rendah. Dalam hal ini perlu dipertimbangkan peran faktor pejamu termasuk faklor genetik maupun faktor lingkungan yang selain mempengaruhi kuman Hp agaknya juga mungkin dapat mempengaruhi fisiologi maupun imunologi pejamu.
Situasi yang berbeda terjadi di Jepang, suatu negarayang maju, dengan prevalensi Hp yang relatif rendah tetapi dengan prevalensi kanker lambung yang tinggi. Dari sisikuman Hp diketahui terdapat beberapa strain yanglebih virulen sehingga selalu ditemukan pada pasien dengan tukak peptik, gastritis kronik, maupun kanker lambung. Gen Vac A selalu dapat ditemukan pada kuman Hp, tetapi tidak semuanya menghasilkan sitotoksin. Ternyata struktur gen ini sangat heterogen di mana pada strain penghasil sitotoksin yang linggi terdapat sekuen signal yang tertentu.
Gen CagA hanya ditemukan pada sebagian strain, dan merupakan salah satu dari kelompok yang terdiri dari 20 gen lain, membentuk apa yang disebut sebagai pulau patogenesitas ( pathogenicity island). Asosiasi antara CagA dengan tukak peptik atau kanker lambung mungkin melalui respons inflamasi yang meningkat terhadap Hp yang mengandung CagA.
Untuk tukak peptik, CagA merupakan petanda yang paling baik, tetapi di daerah dengan prevalensi CagA yang tinggi tidak mungkin untuk membuktikan asosiasi tersebut dengan melakukan suatu panelitian kasus kelola. Berbagai strain Hp menghasilkan vacuolating cytotoxin, mengandung kluster gen CagA yang dapat menginduksi IL-S. Protein CagA dan gen CagA mungkin merupakan satu petanda straln yang ulserogenik dan karsinogenik. Di Jepang. antibodi anti CagA tidak memberi petunjuk yang berguna terhadap kemungkinan kelainan tersebut. Struktur gen CagA daur strain yang menyebabkan tukak lambung dan tukak duodenum di Jepang sangat berbeda. Hal tersebut memberi petunjuk perlunya diketahui profil antibodi anti CagA secara lebih rinci untuk dapat menjelaskan makna klinis strainHp tersebut.
Penelitian diversitas genetik Hp dan interaksi dengan respons antibodi pejamu merupakan kunci untuk memahami diversitas penyakit akibat infeksi Hp. Di Indonesia belum ada data penelitian tentang prevalensi infeksi strain Hp, tetapi di masa depan hal ini perlu dilakukan agar dapat ditetapkan hubungannya dengan kelainan patologis saluran cerna bagian atas.
Patogenesis
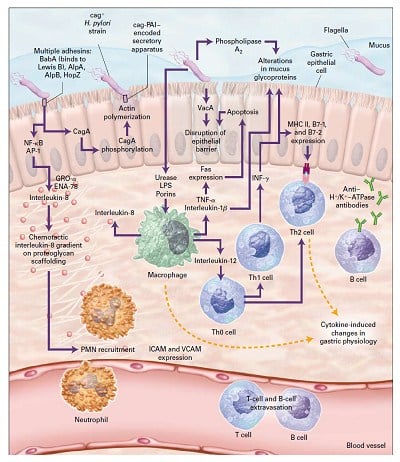
Mukosa gaster terlindungi sangat baik dari infeksi bakteri, namun H. Pylori memiliki kemampuan adaptasi yang sangat baik terhadap lingkungan ekologi lambung, dengan serangkaian langkah unik masuk ke dalam mukus, berenang dan orientasi spasial di dalam mukus, melekat pada sel epitel lambung, menghindar dari respons immun, dan sebagai akibatnya terjadi kolonisasi dan transmisi persisten.
Setelah memasuki saluran cerna, baktei H. Pylori harus menghindari aktivitas bakterisidal yang terdapat dalam isi lumen lambung, dan masuk ke dalam lapisan mukus. Produksi urease dan motilitas sangat penting berperan pada langkah awal infeksi ini. Urease menghidrolisis urea menjadi karbondioksida dan ammonia, sehingga H. Pylori mampu bertahan hidup dalam lingkungan yang asam. Aktivitas enzim ini diatur oleh suatu saluran urea yang tergantung pH (PH-gated urea channel), Ure-I, yang terbuka pada pH yang rendah, dan menutup aliran urea pada keadaan netral. Motilitas bakteri sangat penting pada kolonisasi, dan flagel H. Pylori sangat baik beradaptasi pada lipatan-lipatan/relung-relung lambung.
Pylori dapat terikat /melekat erat pada sel-sel epitel melalui berbagai komponen permukaan bakteri. Adhesin yang sangat dikenal baik karakteristiknya adalah BabA, suatu protein membran luar yang terikat pada group anti- gen darah Lewis B. Beberapa protein lain famili Hop protein (protein membran luar) juga merupakan mediasi adhesi pada sel epitel. Bukti-bukti menunjukkan bahwa adhesi, terutama oleh BabA, sangat relevan dengan penyakit- penyakit terkait H. Pylori dan dapat mempengaruhi derajat beratnya penyakit, meskipun beberapa hasil studi terdapat pula yang bertentangan.Sebagian besar strain H. Pylori mengeluarkan suatu eksotoksin, Vac A (vacuolating cytotoxin). Toksin tersebut masuk ke dalam membran sel epitel dan membentuk suatu saluran tergantung voltase, suatu anion hexamer selektif, yang mana melalui saluran tersebut bikarbonat dan anion- anion organik dapat dilepaskan, tampaknya juga untuk menyediakan nutrisi bagi bakteri.
VacA juga menyerang membran mitikondria, sehingga menyebabkan lepasnya sitokrom c dan mengakibatkan apoptosis. Peran patogenik dari dari toksin masih diperdebatkan. Pada studi-studi hewan, bakteri mutan tanpa VacA juga dapat melakukan kolonisasi , dan strain dengan gen VacA yang inaktif telah pula diisolasi dari pasien-pasien, menunjukkan bahwa VacA tidak esensial untuk kolonisasi. Namun demikian, mutan tanpa VacA kalah kompetisi dari wild-type bakteri pada suatu studi pada tikus, menunjukkan bahwa VacA meningkatkan vitalitas bakteri. Analisis peran VacA dipersulit oleh kenyataan variabilitas VacA yang luas. Di negara-negara barat, varian gen-gen VacA tertentu berhubungan dengan keadaan penyakit yang lebih berat. Namun demikian, hubungan seperti itu tidak ditemukan di Asia, dan dasar fungsional yang mendasari hubungan tersebut tidak diketahui.
Beberapa strain H. Pylori memllikt cag-PAI (cag pathogenicity island), suatu fragmen genom yang mengandung 29 gen. Beberapa gen ini menyandi komponen-komponen sekresi yang men-translokasi CagA kedalam sel pejamu. Setelah memasuki sel epitel, CagA difosforilasi dan terikat pada SHP-2 tirosin fosfatase, menimbulkan respons selular growthfactor-like danproduksi sitokil oleh sel pejamu.
Baca Juga Artikel Yang Mungkin Berhubungan : Reproduksi Virus – Pengertian, Cara, Strategi, Bakteriofage, Virus Hewan, Contohnya
Respons Pejamu Terhadap H.Pylori
Pylori menyebabkan peradangan lambung yang terus- menerus. Respon peradangan ini mula-mula terdiri dari penarikan neutrofil, diikuti limfosit T dan B, sel plasma, dan makrofag, bersamaan dengan terjadinya kerusakan sel epitel. Karena H. Pylori sangat jarang menginvasi mukosa gaster, respon pejamu terutama dipicu oleh menempel/ melekatnya bakteri pada sel epitel. Patogen tersebut dapat terikat pada molekul MHC c/ass 11 di permukaan sel epitel gaster dan menginduksi terjadinya apoptosis. Perubahan lebih lanjut dalam sel epitel tergantung pada protein-protein yang disandi pada cag-PAI dan translokasi CagA kedalam sel epitel gaster. Urease H. Pylori dan porin juga dapat berperan pada terjadinya ekstravasasi dan kemotaksis neutrofil.
Epitel gaster pasien yang terinfeksi H. Pylori meningkatkan kadar interleukin-1B, interleukin-2, interleukin-6, interleukin-8, dan tumor nekrosis faktor alfa. Di antara semua itu, interleukin-S, suatu neutrophil-acti- vating chemokine yang poten yang diekspresikan oleh sel epitel gaster, tampaknya berperan penting. Shain 11. Pylori yang mengandung cag-PAl menimbulkan respons interleukin-8 yang jauh lebih kuat dibandingkan strain yang tidak mengandung cag, dan respons ini tergantung pada aktivasi nuclear factor-rcB (NF-KB) dan respons segera dari faldor transkripsi activator protein I (AP-l).
Infeksi H. Pylori merangsang timbulnya respons humoral mukosa dan sistemik. Produksi antibodi yang terjadi tidak dapat menghilangkan/eradikasi infeksi, bahkan menimbulkan kerusakan jaringan. Pada beberapa pasien yang terinfeksi H. Pylorl timbul respons autoantibodi terhadap H+/I(+-ATPase sel-sel parietal lambung yang berkaitan dengan meningkatnya atrofi korpus gaster.
Selama respons immun spesifik, subgroup sel T yang berbeda timbul. Sel-sel ini berpartisipasi dalam proteksi mukosa lambung, dan membantu membedakan antara bakteri patogen dan komensal. Sel T helper immatur (Th 0) berdiferensiasi menjadi 2 subtipe fungsional: sel Th-1, mensekresi interleukin 2 dan interferon gamma; dan Th-2, mensekresi IL4, IL-5, dan IL- 10. Sel Th2 menstimulasi sel B sebagai respons terhadap patogen ekstrasel, sedangkan Thl terutama timbul sebagai respons terhadap patogen intrasel. Karena H. Pylori bersifat tidak invasif dan merangsang timbulnya respons humoral yang kuat, maka yang diharapkan adalah respons sel TM. Namun timbul paradoks, sel-sel mukosa gaster yang spesifik terhadap H. Pylori umumnya justru menunjukkan fenotip Thl. Studi- studi menunjukkan bahwa sitokin Thl menyebabkan gastritis, sedangkan sitokin Th2 protektis terhadap peradangan lambung. Orientasi Thl tersebut tampaknya meningkatkan produksi interleukin-l8 di antrum sebagai respons terhadap infeksi H. Pylori. Bias Thl tersebut, bersama dengan apoptosis yang dimediasi Fas, menyebabkan infeksi H. pylori menjadi persisten.
Kerusakan sel epitel lambung juga disebabkan oleh reactive oxygen dan nitrogen species yang dihasilkan oleh neutrofil teraktivasi. Inflamasi kronik juga meningkatkan turn over sel epitel dan apotosis. Polimorfisme proinflamasi dari gen interleukin-lB mengarahkan perkembangan gastritis terutama terjadi di korpus gaster dan berkaitan dengan hipoklorhidria, atrofi gaster, dan adenokarsinoma gaster. Bila polimorfisme proinflamasi tidak ada, gastritis akibat tL Pylori berkembang terutama di antrum, dan berkatan dengan kadar sekrepi asam yang normal atau tinggi.
Baca Juga Artikel Yang Mungkin Berhubungan : Penjelasan Ciri-Ciri Borrelia Burgdorferi Dalam Biologi
Karakteristik Helicobacter Pylori
Karakteristik relevansi klinis patofisiologi infeksi H. Pylori adalah:
- Eksotoksin Vac A disekresi oleh sebagian besar/ mayoritas strain 1L Pylori. Polimorfisme gen Vac A berkaitan dengan keadaan penyakit yang lebih berat.
- Tingginya kadar fosfolipase A (PLA) memungkinkan,F1p memasuki / penetrasi ke dalam mukus Kadar PLA yang tinggi disekresi oleh strain Hp yang diisolasi dari pasien-pasien kanker lambung.
- Hp menyebabkan peradangan pada antrum (antritis) atau korpus (korpusitis) gaster, atau sering pula pada keduanya (pangastritis). Pada antritis, terjadi hipergastrilemia, meningkatnya produksi asam, dan suatu risiko tinggi terjadinya ulkus Mengapa hanya sekitar 2 – 20%o dari antritis yang berkembang menjadi ulkus duodenum masih belum jelas.
- Duodenitis terjadi disebabkan kolonisasi pulau-pulau metaplasia gaster di dalam bulbus duodenum, yang dicetuskan (triggeredl oleh tingginya produksi
- Korpusitis Hp berkaitan dengan ulkus gaster, atrofi mukosa gaster, menurunnya sekresi asam sehingga terjadi 2,5 kali peningkatan risiko kanker
Baca Juga Artikel Yang Mungkin Berhubungan : Jenis, Habitat, Pengertian Bakteri Beserta Bakteri Penyebab Penyakit
Diagnosis Infeksi Helicobacter Pylori
Kuman Helicobacter pylori bersifat mikroaerofilik dan hidup di lingkungan yang unik, dibawah mukus dinding lambung yang bersuasana asam. Kuman ini mempunyai enzim urease yang dapat memecah ureum menjadi amonia yang bersifat basa, sehingga tercipta lingkungan mikro yang memungkinkan kuman ini bertahan hidup. Karena itu prosedur diagnostik cukup sulit karena harus melakukan tindakan yang invasif yaitu dengan melakukan gastroskopi untuk mendapatkan spesimen yang diperlukan untuk pemeriksaan langsung, histopatologi ataupun kultur mikrobiologi. Selain itu terdapat pemeriksaan non invasif seperti tes serologi dan urea breath test (UBT).
Tujuan pemeriksaan diagnostik infeksi Hp adalah untuk menetapkan adanya infeksi sebelum memberikan pengobatan atau untuk penelitian epidemiologi. Selain itu untuk mengamati apakah telah tercapai eradikasi sesudah pemberian obat antibiotik.
Ada 2 macam cara diagnosa infeksi H. pylori yaitu diagnosa invasif yang memerlukan endoskopi dan biopsi mukosa lambung, dan diagnosa noninvasif yang tidak memerlukan endoskopi dan biopsi.
- Diagnosa invasif meliputi :
1. Deteksi kuman H. pylori dengan cara pemeriksaan histopatologik
2. Tes urease cepat yang mendeteksi adanya enzim urease dalam spesimen biopsi lambung.
3. Pembiakan kuman H. pylori dari spesimen biopsi lambung.
4. Pemeriksaan PCR spesimen biopsi lambung - Diagnosa noninvasif meliputi :
1. Tes Nafas Urea (Urea Breath Test) untuk mengukur enzim urease yang ada dalam lambung yang diproduksi oleh kuman H. pylori.
2. Tes Immunoserologic untuk deteksi antibodi terhadap kuman H. pylori dalam darah penderita.
3. Deteksi antigen fekal untuk mendeteksi fragmen kuman H. pylori yang didapatkan dalam tinja.
Serologi
Pemeriksaan serologi banyak digunakan dalam penelitian epidemiologi karena relatif murah dan dapat diterima oleh kelompok pasien asimtomatik atau anak-anak yang tidak mau diperiksa dengan cara yang invasif seperti gastroskopi.
Pada umumnya yang diperiksa adalah antibodi IgG terhadap kuman Helicobacter pylori. Cara ini sering digunakan untuk penetitian epidemiologi atau untuk evaluasi sebelum pemberian terapi eradikasi. Teknik yang dipakai adalah dengan menggunakan ELIS A, Westernblot, fiksasi komplemen, dan imunofluoresen. ELISA paling luas penggunaannya. Studi prevalensi di Indonesia dilakukan dengan menggunakan metode PHA, Sedangkan studi klinik umunnya. menggunakan ELISA.
Dewasa ini secara komersial telah cukup banyak tes ELISA yang tersedia dengan cara penggunaan yang relatif sederhana dan hasil yang akurat. Yang menjadi masalah adalah sensitivitas dan spesifisitas yang bervariasi secara geografis. Hal ini diduga karena pengaruh faktor antigen lokal yang berbeda atau akibat titer yang relatif rendah, misalnya pada kelompok pasien anak atau populasi tertentu. Dengan demikian dianggap perlu untuk melakukan validasi tes sebelum digunakan secara meluas di suatu wilayah. Sebagai contoh, studi di Jakarta menggunakan tes Elisa buatan Roche menunjukkan sensitivitas dan spesifisitas yang relatif lebih rendah dibandingkan dengan laporan dari negara Barat. Untuk meningkatkan sensitivitas dan spesifisitasnya, dapat dilakukan dengan menetapkan cut offpoint sebagai batas hasil yang positif dan negatif dalam suatu populasi. Penelitian di Jakarta menunjukkan, dengan menetapkan cut offpoint 1800 EU/L dapat ditingkatkan sensitivitas tes ELISA.
Dalam perkembangannya cara ELISA telah dipakai pula untuk tes di ruang praktek dokter, in ffice Hp test, dengan cara yang sederhana, tanpa sentrifugasi, bersifat kualitatif dan hasilnya diperoleh dalam waktu 5 – l0 menit.
Selain serum, tes ELISA telah dilakukan pula pada saliva pasien terutama pada anak. Sensitivitas dan spesifisitasnya lebih rendah dibandingkan dengan serum tetapi diduga kadar antibodi dalam saliva menurun lebih awal pasca terapi eradikasi sehingga mungkin dapat digunakan untuk menilai hasil terapi antimikrobial.
Urea Breath Test (UBT)
Pemeriksaan ini merupakan baku emas untuk deteksi infeksi H. pylori secara non invasif yang pertama kali dikemukakan pada tahun 1987 oleh Graham dan Bell. Cara kerjanya adalah dengan menyuruh pasien menelan urea yang mengandung isotop Carbon, baik 13C ataupun l4C. Bila ada aktivitas urease dari kuman H. pylori akan dihasilkan isotop karbon dioksida yang diserap dan dikeluarkan melalui pernapasan. Hasilnya dinilai dengan membandingkan kenaikan ekskresi isotop dibandingkan dengan nilai dasar. Bila hasilnya positif berarti terdapat infeksi kuman H. pylori. l3C merupakan isotop nonradioaktif, ditemukan pada l,ll % karbon dioksida yang keluar melalui udara pernapasan normal. Dianggap positif bila terjadi kenaikan minimal 0,01 % kadar isotop, sehingga dibutuhkan alat mass spectrometer yang sangat sensitif tetapi harganya sangat mahal. Mula-mula diambil sampel udara pernapasan untuk menentukan nilai dasar. Kemudian diberikan tes mealberupacairan dengan kalori tinggi atau larutan 0,1 N asam sitrat untuk memperlambat pengosongan lambung sehingga kontak antara isotop dengan mukosa lambung lebih baik.
Dosis 13C yang diberikan adalah dalam bentuk urea sebanyak 75-100 mg yang memberikan akurasi lebih dari Terdapat berbagai modifikasi protokol sehingga setiap perubahan memerlukan validasi untuk mempertahankan akurasi pemeriksaan.
Isotop 14 C memancarkan radiasi yang dapat dianalisis dengan scintillation counter. Pengambilan sampel dilakukan sesudah 10 dan 20 menit baik dengan atau tanpa tes meal. Cara ini relatif murah, tetapi harus diperhatikan standar keamanan yang baik, walaupun sebenamya dosis radiasi sangat kecil. Cara ini tidak dianjurkan pada perempuan hamil ataupun anak-anak.
Dalam hal akurasi, kedua cara ini setara, dengan sensitivitas dan spesifisitas lebih dari 90 %. Hasil positif palsu harus dipertimbangkan bila diduga ada mikroorganisme lain yang juga menghasilkan urease pada keadaan aklorhidria. Hasil negatifpalsu dapat terjadi bila pasien mendapat antibiotik. antasid- bismuth. atau anti sekresi asam. Karena itu dianjurkan unruk menghentikan obat tersebut dua minggu sebelum dilakukan pemeriksaan. Penggunaan UBT mempunyai kelebihan dibandingkan dengan tes yang meng-eunakan spesimen biopsi karena mewakili seluruh permukaan mukosa lambung. Aplikasi klinis digunakan untuk deteksi infeksi pada studi epidemiologi dan individu pasien dan konfirmasi keberhasilan terapi eradikasi yang dilakukan sesudah 4 Minggu kemudian.
Dapat disimpulkan bahwa indikasi tes serologi dan UBT agak tumpang tindih, sehingga pemanfaatannya harus disesuaikan dengan tujuan yang ingin dicapai. Pemeriksaan serologi lebih mudah, murah sehingga sangat cocok untuk suatu penelitian populasi yang luas. Pemeriksaan UBT tidak memerlukan validasi lokal, menetapkan adanya infeksi yang aktif, dan merupakan pemeriksaan baku emas untuk konfirmasi hasil terapi eradikasi. Dengan adanya pemeriksaan noninvasif, terbuka kesempatan untuk melakukan penatalaksanaan pasien dispepsia ditingkat pelayanan primer oleh dokter umum, dengan memperhatikan latar belakang prevalensi infeksi H. pylori sertapenyakit yang menyertainya, terutama tukak peptik dan keganasan lambung.
Pemeriksaan lnvasif
Pemeriksaan invasif untuk diagnosis infeksi H. Pylori dilakukan dengan mengambil spesimen biopsi mukosa lambung secara endoskopik. Selanjutnya spesimen yang diambil dengan persyaratan dan cara tertentu akan diperiksa dengan teknik khusus sesuai dengan tujuan diagnostik yatg akan dicapai. Persyaratan yang dimaksudkan adalah upaya untuk mengurangi kemungkinan terjadinya hasil negatif palsu akibat pengaruh obat-obatan yang dipergunakan sebelum pengambilan sampel biopsi. Biasanya dianjurkan untuk menghentikan obat antibiotik, anti sekresi asam lambung terutama golongan inhibitor pompa proton, bismuth selama satu atau dua minggu sebelum pemeriksaan. Biopsi standar untuk diagnosis infeksi H. pylori diambil dari antrum (2) dankorpus (2), sedangkan untuk menilai adanya metaplasia intestinal biasanya diambil biopsi pada angulus. Spesimen untuk kultur mikrobiologi harus diambil pertama kali karena harus dilakukan secara steril. kemudian untukbiopsy urease test dan histopatologi.
Biopsy Urease Test (BUT)
Tersedia berbagai pilihan mulai yang dibuat sendiri dalam bentuk cairan ataupun padat seperti tes CLO. Dasarnya adalah adanya enzim urease dari kuman H. pylori yang mengubah urea menjadi amonia yang bersifat basa sehingga terjadi perubahan warna media menjadi merah. Hasilnya dapat dibaca dalam beberapa menit sampai 24 jam, dan pengambilan lebih dari satu spesimen akan meningkatkan akurasi pemeriksaan ini. Sensitivitas pemeriksaan ini sekitar 89-98% sedangkan spesifisitasnyamencapai l00%.
Penggunaan antibiotik atau penghambat pompa proton akan menghambat pertumbuhan kuman sehingga harus dihentikan satu minggu sebelumnya. Cara ini tidak dapat digunakan untuk menilai hasil pengobatan terapi eradikasi.
Histopathology
Pemeriksaan histopatologi dapat digunakan untuk mendeteksi infeksi H. pylori serta menilai derajat inflamasi gastritis.Pemeriksaan standar dengan pewarnaan H & E untuk deteksi kuman mempunyai sensitivitas 93 % dari spesifisitas 87% dengan akurasi 92o/o.Pewarnaan khusus secara Giemsa, Genta atau Warthin-Starry memberikan gambaran H. pylori yang lebih jelas, sedangkan dengan pewarnaan Genta gambaran metaplasia gastrik akan tampak lebih jelas. Densitas kuman akan menurun bila sebelumnya diberikan obat antibiotik atau inhibitor pompa proton, sehingga akan menurunkan sensitivitas pemeriksaan.
Biakan Mikrobiologi
Dalam penatalaksanaan penyakit akibat infeksi H. pylori. kultur tidak dilakukan secara rutin karena dua alasafi. Cara diagnostik lain baik yang non invasif maupun yang invasif memberikan hasil yang memuaskan dengan akurasi yang tinggi. Selain itu pemeriksaan kultur sendiri tidak mudah dilakukan, dengan sensitivitas yang relatif rendah, berkisar Antara 66-98 %. Teknik yang dianjurkan adalah dengan tes difusi agar atau dengan E test di mana sekaligus dapat ditentukan konsentrasi inhibisi minimal dari antibiotik yang diuji. Pemeriksaan kultur akan sangat membantu untuk pengobatan kegagalan terapi eradikasi, sehingga dapat dipilih antibiotik yang sesuai.
Polymerase Chain Reaction (PCR)
Polymerase Chain Reaction merupakan pilihan yang menarik karena sensitivitas yang tinggi (94-100%) serta spesifisitas yang tinggi pula (100 % Bahan yang digunakan adalah spesimen biopsi baik yang sudah diparafin maupun bekas tes urease seperti CLO. Keuntungannya adalah kemampuannya unfuk mendeteksi infeksi dengan densitas yang rendah, bahkanjuga ekspresi dari berbagai gen bakteri seperti Cag.A. Selain biopsi mukosa lambung, PCR dapat pula mendeteksinfeksi H. pylori dengan memeriksa cairan lambung, yang perlu dijaga jangan sampai terjadi kontaminasi baik dari skop endoskopi maupun dari rongga mulut atau plak gigi karena dapat memberikan hasil positif palsu. PCR dapat juga dipergunakan untuk menilai hasil terapi eradikasi . Cara ini termasuk pemeriksaan yang canggih dengan biaya yang cukup mahal.
Baca Juga Artikel Yang Mungkin Berhubungan : Ciri-Ciri Bakteri Mycoplasma Dalam Biologi
Infeksi Hp, Gastritis dan Sekresi Asam Lambung
Terdapat hubungan timbal balik antara infeksi Helicobacter pylori, gastritis dengan asam lambung. Infeksi Hp yang predominan di antrum akan meningkatkan sekresi asam lambung dengan konsekuensi terjadinya tukak duodenum. Inflamasi pada antrum akan menstimulasi sekresi gastrin, yang selanjutnya akan merangsang sel parietal untuk meningkatkan sekresi asam lambung. Infeksi Hp akan meningkatkan kadar Gastrin, yang terutama berasal dari mukosa antrum. Selain itu peningkatan sekresi gastrin juga terjadi akibat menurunnya kadar somatostatin dalam mukosa antrum, yang berasal dari sel D. Dalam hal ini secara fisiologis somatostatin atau sel D berfungsi sebagai acid brake, menekan fungsi sel G dan sekresi asam lambung oleh sel Parietal. Mekanisme lain adalah melalui peran sitokin lokal akibat inflamasi antrum yang juga dapat mempengaruhi sekresi somatostatin maupun gastrin.
Apabila gastritis akibat infeksi Hp predominan di korpus, sekresi asam lambung akan menurun, dengan risiko jangka panjang yang lebih besar untuk menjadi kanker lambung. Inflamasi korpus yangberat atau luas, akan mengganggu atau menekan fungsi sel parietal yang menimbulkan hipo atau aklorhidria, biasanya disertai pula dengan atrofi mukosa korpus, yang merupakan lesi premaligna untuk terjadinya keganasan lambung. Sebaliknya, tingkat sekresi asam lambung yang mungkin dipengaruhi faktor genetik diduga berperan temadap perbedaan predominasi gastritis akibat infeksi Hp. Bila sekresi asam lambung tinggi, akan terjadi gastritis predominan antrum, sedangkan bila rendah akan terjadi gastritis predominan korpus dengan akibat penyakit yang berbeda.
Manifestasi Klinis
Seperti telah dikemukakan. manifestasi klinis akan sangat bervariasi mulai dari tanpa gejala, dispepsia fungsional,tukak peptik sampai kanker lambung. Karena lamanya hasil pembiakan H. pylori maka untuk mendapatkan hasil yang cepat maka sering digunakan rapid urease test, yang lebih dikenal dengan CLO test (CLO adalah singkatan dari Campylobacter Like Organism). Dalam tes ini spesimen biopsi mukosa lambung dimasukkan dalam medium agar yang dicampur urea dan indikator. Bila dalam bahan biopsi tersebut mengandung urease maka akan terjadi perubahan warna dari kuning menjadi merah.
Sebagian besar individu yang terkena infeksi H. pylori tidak mengalami keluhan walaupun pada pemeriksaan biopsi mukosa lambung pada kasus-kasus asimptomatik sebagian besar didapatkan gambaran gastritis kronik aktif.
- Dyspepsia dengan gambaran endoskopik yang bermacam-macam, mulai dari normal sampai dengan ulkus lambung atau ulkus duodeni, gastritis, duodenitis, gastritis atrofik, gastritis hypertrofik.
- MALT (Mucosal Associated Lifoid Tissue) limfoma dan kanker lambung di bagian destal (tipe intestinal).
Cara penegakkan diagnosa yang banyak dipakai dengan hasil yang baik adalah dengan diagnosa histologis Cara lain adalah tes napas urea (urea breath test) dan pemeriksaan serologik. Kedua cara ini tidak memerlukan endoskopi. Belakangan ini ditemukan cara diagnosa infeksi H. pylori dengan cara deteksi antigen kuman H. pylori pada tinja penderita dengan metoda Elisa
Baca Juga Artikel Yang Mungkin Berhubungan : Virus Pemakan Bakteri ( Bakteriofag ) Beserta Penjelasannya
Indikasi dan Evolusi Helicobacter Pylori
Indikasi Terapi Eradikasi Helicobacter Pylori
Sangat Dianjurkan. Ulkus duodeni, ulkus ventrikuli, MALT Lymphoma gaster derajat keganasan rendah, riwayat kanker lambung di keluarga, gastritis kronik aktif (gambaran PA), Paska reseksi kanker lambung dini, gastritis atrofik.
Dianjurkan. Keinginan pasien untuk diobati setelah mendapat penjelasan yang memadai, dispepsia fungsional (tidak ditemukan kelainan perendoskopi, biokimiawi, atau laboratorium), gastropati obat anti inflamasi non steroid (OAINS), gastroesophageal reflux disease (GERD) yang memerlukan terapi antisekresi asam jangka panjang.
Evolusi Terapi Eradikasi Helicobacter Pylori
Pada dasarnya dikenal terapi kombinasi yang didasarkan pada obat bismuth dan terapi yang didasarkan pada penghambat pompa proton (PPI). Mula-mula digunakan senyawa bismuth sebagai obat tunggal, dengan hasil yang kurang memuaskan sehingga dikembangkan terapi kombinasi dual, tripel bahkan terapi kuadrapel. Waktu pemberian juga terus diusahakan untuk diberikan sesingkat mungkin mulai dari 4, 2, dan dewasa ini umumnya dianjurkan untuk waktu satu minggu. Perkembangan ini sangat mendukung kepatuhan pasien, karena selain efektivitas yang cukup tinggi, kemungkinan efek samping menjadi lebih kecil. Walaupun relatif cukup mahal, terapi kombinasi dinilai cukup cost effective terutama karena dapat menekan angka kekambuhan dalam jangka panjang, misalnya dalam pengobatan tukak duodeni dan tukak lambung.
Baca Juga Artikel Yang Mungkin Berhubungan : Penjelasan Reproduksi Bakteri Dalam Ilmu Biologi
Pengobatan dan Terapi Helicobacter Pylori
Terapi Eradikasi
Laporan uji klinis terapi infeksi Hp di Indonesia pada mulanya menggunakan monoterapi menggunakan preparat bismuth dengan tujuan supresi dan bukan eradikasi. Dewasa ini regimen terapi yang digunakan adalah terapi
Tabel 2. Peran infeksi HP Pada berbagai penyakit gastroduodenal
|
Faktor Etiologi utama |
Prevalensi |
| Tukak duodenum | 100% |
| Tukak lambung | 80-90% |
| Gastritis Kronik | 40% |
kombinasi antara penghambat pompa proton dengan dua atau tiga macam antibiotik. Pertemuan konsensus nasional penatalaksanaan infeksi Helicobacter pylori di Jakarta pada bulan Januari 2003 menganjurkan regimen terapi sebagai berikut:
Terapi lini pertama / terapi tripel
• Urutan Prioritas
- PPI +Amoksisilin + klaritromisin
- PPI + Metronidazol + klaritromisin
- PPI + Metronidazol + tetrasiklin
Pengobatan dilakukan selama 1 minggu
• Dosis
- Proton Pump Inhibitor
Omeprazole 2x20mg
Lansoprazole 2x30mg
Rabeprazole 2x l0mg
Esomeprazole 2x20mg - Amoksisilin :2x l000mg/hari
- Klaritromisin :2x500mg/hari
- Metronidazol : 3x500mg/hari
- Tetrasiklin : 4x250mg/hari
Terapi lini kedua / terapi kuadrupel
Terapi lini kedua dilakukanjika terdapat kegagalan pada lini pertama. Kriteria gagal : 4 minggu pasca terapi, kuman H. Pylori tetap positif berdasarkan pemeriksaan I-IBT/ HpSA atau histopatologi.
- Urutan prioritas
– Collodial bismuth subcitrate +PPl+ Amoksisilin +klarihomisin
– Collodial bismuth subcitrate + PPI + Metronidazol+ Klaritromisin
– Collodial bismuth subcitrate +PPI + Metronidazol+ TetrasiklinPengobatan dilakukan selama I minggu. - Dosis collodial bismuth subcitrate.’ 4 x 120 mg Bila terapi lini kedua gagal, sangat dianjurkan pemeriksaan kultur dan resistensi H. Pylori dengan media transport MIU.
- Regimen antibiotika yang baru
Timbulnya resistensi terhadap antibiotika menyebabkan kesulitan dalam pemilihan regimen terapi lini kedua. Oleh karena itu, seleksi terapi lini pertama harus sudah mempertimbangkan pula pilihan regimen terapi lini kedua yang mungkin akan diimplementasikan bila regimen terapi lini pertama gagal. Regimen terapi dengan efektivitas eradikasi > 80% yang dianjurkan untuk digunakan pada praklek klinis. Pada pasien-pasien yang gagal dengan regimen terapi dengan basis klaritromisin, regimen kombinasi terdiri dari lansoprazol 2×30 mg, amoksisilin 2 x I gram, dan levofloksasin 2 x 200 mg Dilaporkan menunjukkan eradikasi 69%. Levofloksasin dapat pula diberikan dengan dosis I x 500 mg. Kombinasi lain yang dilaporkanefektif adalah PPI bid, rifabutin 300 mg qd (lx sehari), dan amoksisilin 2 x I gram. Dhekomendasikan untuk menggunakan kombinasi PAC (PPI – Amoxycillin- Clarithromycin) sebagai terapi lini pertama, dan bila gagal dapat dilanjutkan dengan terapi kuadrupel seperti P-BMT (PPl-Bismuth-Metronida- zole-Tetracyclln). Namun, pada komunitas dengan prevalensi tinggi resistensi terhadap makrolid (> 20% resisten terhadap klaritromisin), terapi lini pertama sebaiknya terapi kuadrupel. Studi metanalisis terapi kuadrupel sebagai terapi lini pertama menunjukkan tingkat eradikasi lebih dari 85%, bahkan pada area dengan resistensi terhadap metronidazol yang tinggi, dan 69% lebih efektif dibandingkan PAC pada keadaan terdapat resistensi terhadap klaritromisin. Analisa cost effective terapi tripel atau terapi kuadripel tampak serupa, namun terapi kuadrupel tampaknya sedikit lebih cost-effective.
Fluoroquinolon atau Rifabutin dalam kombinasi bersama amoksisilin dan PPI menunjukkan hasil yang menjanjikan. Terapi dengan fufabutin 2 x 150 mg, Amoksisilin 2 x I gram, dan om eprazol2 x20 mg selama 14 hari menunjukkan eradikasi 7 2oh padapasien-pasien yang gagal dengan kombinasi terapi PAC dan P-BMT. Terapi lini pertama dengan LAE, yaitu levofloksasin 1 x 500 mg, azitromisin I kali 500 mg, dan esomeprazol 2x 20 mg selama 7 hari lebih efektif (93,3%) dibandingkan terapi standar tripel EAC (70%). Terapi lini kedua helicobacter pylori RLA, yaitu rabeprazol2 x20 mg, levofloksasin I x 500 mg, dan amoksisilin 2 x I gram selama 12 hari sama efektiftya denganterapi kuadrupel R-BMI namun lebih ditoleransi dengan baik dan menunjukkan compliance serta tingkat kepatuhan minum obat yang tinggi. Terapi tripel selama 10 hari dengan levofloksasin, esomeprazol, amoksisilin / azitromisin lebih efektif (86,6% /80%) dibandingkan regimen klasik E-BMT (71,4%) dan menunjukkan compliance yang lebih baik.
Kriteria Keberhasilan Terapi Eradikasi
Empat minggu setelah terapi selesai, dilakukan pemeriksaan UBT/HpSA atau histopatologi. Jika UBT negatif atau PA negatif terapi dianggap berhasil (sembuh).
Terapi kombinasi tersebut dianjurkan untuk diberikan selama satu minggu. Mengingat cepatnya terjadi resistensi Hp terhadap antibiotik, kiranya perlu diadakan penelitian pola resistensi di Indonesia secara berkala agar dapat menjadi dasar pilihan antibiotik yang tepat. Masalah lain adalah penilaian keberhasilan eradikasi yang harus menggunakan metoda diagnostik yang paling peka dan non invasif, terutama untuk penelitian epidemiologis. Selain standar emas kultur mikrobilogi agaknya pemeriksaan tes Pernapasan urea (urea breath test l3C atau l4C) perlu diadakan dan digunakan secara meluas.
Dari segi biaya, regimen terapi dengan eradikasi lebih dari 90 % akan menyembuhkan tukak peptik, tanpa perlu terapi pemeliharaan sehingga leblh cost effective dibandingkan dengan terapi konvensional. Terapi tripel pada awalnya jelas lebih mahal, tetapi dalam jangka panjang akan lebih murah. apalagi bila diperhitungkan peningkatan kualitas hidup, terbebas dari keluhan dan gangguan penyakit.
Yang dimaksudkan eradikasi adalah hilangnya kuman pada pemeriksaan 4 minggu pasca terapi yang dibuktikan dengan metoda yang paling akurat. Dalam perkembangamya dikenal terapi mono, dual, tripel dan kuadripe (tabel2). Dewasa ini dianjurkan adalah terapi kombinasi dengan penyembuhan lebih dari 90%.
Kesepakatan yang dirumuskan dalam konsensus nasional merupakan petunjuk yang dapat digunakan bersama, sekaligus memberikan kemungkinan untuk mendapat data penelitian yang bersifat nasional tentang infeksi Helicobacter pylori di Indonesia. Pola terapi ideal yang mencakup efektivitas, keamalan, kepatuhan dan cost effectiveness mungkin belum ada, tetapi harus diupayakan terapi optimal yang sesuai dengan lingkungan dan kondisi pasien.
Tabel 3. Terapi Eradikasi Helicobacter Pylori
|
Jenis Terapi
|
Eradikasi |
| Terapi Mono
|
|
| Bismuth subsalisilat | 5-10% |
| Colloidal bismuth subcitrate (BSS) | 10-25% |
| Amoksisilin | 15-25% |
| Klaritromisin | 50% |
| lnhibitor pompa proton (lPP) | 0-15% |
|
Terapi Dual |
|
| Bismuth/amoksisilin | 30-60% |
| Bismuth/metronidazol | 30-60% |
| Amoksisilin/metronidazol | 55-95% |
| IPP/Amoksisilin | 55-95% |
| IPP/klaritromisin | 70-90% |
| Ranitidin bismuth sitrat | 70-80% |
| Terapi Tripel
|
|
| Bismuth/metro/tetra | 80-95% |
| IPP/metro/amoksilin atau klaritromisin | 70-95% |
| I PP/amoksilin/klaritromisin
|
70-90% |
| Ranitidin/bismuth sitraVamoksilin,klaritromisin
|
80-90% |
| Terapi Kuadrupel | |
| Bismuthimetro/tetra/l PP | >90% |
Baca Juga Artikel Yang Mungkin Berhubungan : Ciri Ciri Bakteri
Ciri dan Tanda Helicobacter Pylori
Ciri-Ciri Helicobacter Pylori
Pada bakteri Helicobacter pylori ini ditemukan dalam saluran pencernaan manusia, bahkan ditemukan dalam saluran pencernaan pada bagian atas. Bakteri ini dapat ditemukan di usus sekitar 50% orang di dunia. Helicobacter pylori merupakan organisme penyebab pada 80% kasus ulkus lambung di dunia.
Infeksi Helicobacter pylori ini kebanyakan ditemukan di negara-negara dengan sanitasi yang buruk. Mereka yang terinfeksi oleh Helicobacter pylori rentan untuk mengembangkan kanker perut. Untuk gejala utama infeksi ialah sakit perut dan gastritis, bakteri Gram-negatif ini berbentuk heliks, memiliki panjang dan diamter 3 mikrometer dan o,5 mikrometer masing-masing. Pada Bakteri Helicobacter pylori ini biasanya tidak dapat menimbulkan masalah di masa kecil.
Namun, apabila tidak segera ditangani maka akan dapat menyebabkan penyakit pencernaan, termasuk gastritis (iritasi dan peradangan pada selpaut lambung), penyakit ulkus peptikum (ditandai dengan lukan yang terbentuk pada lambung atau bagian atas dari usus kecil yang disebut duodenum), dan bahkan kanker lambung di kemudian hari. Bakteri ini ditemukan di seluruh dunia, terutama di negara-negara berkembang di mana sampai dengan 10% dari anak-anak dan 80% orang dewasa dapat memiliki bukti laboratorium infeksi H. pylori biasanya tanpa gejala.
Tanda Dan Gejala
Dalam hal ini siapapun dapat saja mengalami infeksi H. pylori tanpa menyadarinya karena kebanyakan infeksi H. pylori ini bersifat “diam” dan tidak menghasilkan gejala. Yang ketika bakteri yang menyebabkan gejala, mereka biasanya baik gejala gastritis atau penyakit ulkus peptikum.